添付文書番号
2590009F1136_1_02
企業コード
480235
作成又は改訂年月
日本標準商品分類番号
87259
薬効分類名
前立腺肥大症に伴う排尿障害改善剤
承認等
販売名
ナフトピジル錠25mg「トーワ」
販売名コード
販売名英字表記
NAFTOPIDIL TABLETS 25mg“ TOWA”
承認番号等
販売開始年月
貯法、有効期間
基準名
規制区分
販売名
ナフトピジル錠50mg「トーワ」
販売名コード
販売名英字表記
NAFTOPIDIL TABLETS 50mg“ TOWA”
承認番号等
販売開始年月
貯法、有効期間
基準名
規制区分
販売名
ナフトピジル錠75mg「トーワ」
販売名コード
販売名英字表記
NAFTOPIDIL TABLETS 75mg“ TOWA”
承認番号等
販売開始年月
貯法、有効期間
基準名
規制区分
一般的名称
ナフトピジル錠
禁忌(次の患者には投与しないこと)
組成・性状
組成
ナフトピジル錠25mg「トーワ」
有効成分 | 1錠中 |
|---|
有効成分 | 日局 ナフトピジル
25mg |
|---|
添加剤 | 乳糖水和物、結晶セルロース、デンプングリコール酸ナトリウム、ポビドン、軽質無水ケイ酸、ステアリン酸マグネシウム |
|---|
ナフトピジル錠50mg「トーワ」
有効成分 | 1錠中 |
|---|
有効成分 | 日局 ナフトピジル
50mg |
|---|
添加剤 | 乳糖水和物、結晶セルロース、デンプングリコール酸ナトリウム、ポビドン、軽質無水ケイ酸、ステアリン酸マグネシウム |
|---|
ナフトピジル錠75mg「トーワ」
有効成分 | 1錠中 |
|---|
有効成分 | 日局 ナフトピジル
75mg |
|---|
添加剤 | 乳糖水和物、結晶セルロース、デンプングリコール酸ナトリウム、ポビドン、黄色三二酸化鉄、軽質無水ケイ酸、ステアリン酸マグネシウム |
|---|
製剤の性状
ナフトピジル錠25mg「トーワ」
| 剤形 | 割線入りの素錠 |
|---|
| 色調 | 白色 |
|---|
| 外形 | 表面 裏面 側面 |
|---|
| 大きさ | 大きさ(直径) 6.6mm 大きさ(厚さ) 3.2mm |
|---|
| 質量 | 111mg |
|---|
| 識別コード | Tw024 |
|---|
ナフトピジル錠50mg「トーワ」
| 剤形 | 割線入りの素錠 |
|---|
| 色調 | 白色 |
|---|
| 外形 | 表面 裏面 側面 |
|---|
| 大きさ | 大きさ(直径) 8.6mm 大きさ(厚さ) 4.0mm |
|---|
| 質量 | 222mg |
|---|
| 識別コード | Tw073 |
|---|
ナフトピジル錠75mg「トーワ」
| 剤形 | 割線入りの素錠 |
|---|
| 色調 | 黄白色~淡黄色 |
|---|
| 外形 | 表面 裏面 側面 |
|---|
| 大きさ | 大きさ(直径) 9.6mm 大きさ(厚さ) 4.8mm |
|---|
| 質量 | 333mg |
|---|
| 識別コード | Tw074 |
|---|
効能又は効果
用法及び用量
通常、成人にはナフトピジルとして1日1回25mgより投与を始め、効果が不十分な場合は1~2週間の間隔をおいて50~75mgに漸増し、1日1回食後経口投与する。
なお、症状により適宜増減するが、1日最高投与量は75mgまでとする。
重要な基本的注意
起立性低血圧があらわれることがあるので、体位変換による血圧変化に注意すること。
本剤の投与初期又は用量の急増時等に、起立性低血圧に基づくめまい、立ちくらみ等があらわれることがあるので、高所作業、自動車の運転等危険を伴う作業に従事する場合には注意させること。
本剤投与開始時に降圧剤投与の有無について問診を行い、降圧剤が投与されている場合には血圧変化に注意し、血圧低下がみられたときには、減量又は中止するなど適切な処置を行うこと。
特定の背景を有する患者に関する注意
合併症・既往歴等のある患者
重篤な心疾患のある患者
使用経験がない。
重篤な脳血管障害のある患者
使用経験がない。
肝機能障害患者
健常人に比し、最高血漿中濃度が約2倍、血漿中濃度曲線下面積が約4倍に増加したとの報告がある。
高齢者
低用量(例えば12.5mg/日等)から投与を開始するなど、患者の状態を観察しながら慎重に投与すること。本剤は、主として肝臓から排泄されるが、高齢者では肝機能が低下していることが多いため、排泄が遅延し、高い血中濃度が持続するおそれがある。
相互作用
併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|
利尿剤
降圧剤
| 降圧作用が増強するおそれがあるので、減量するなど注意すること。 | 本剤及び併用薬の降圧作用が互いに協力的に作用する。 |
ホスホジエステラーゼ5阻害作用を有する薬剤 シルデナフィルクエン酸塩、バルデナフィル塩酸塩水和物等 | 併用により、症候性低血圧があらわれるおそれがある。 | これらは血管拡張作用による降圧作用を有するため、併用により降圧作用を増強するおそれがある。 |
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
重大な副作用
肝機能障害、黄疸 (頻度不明)
AST、ALT、γ-GTP等の上昇を伴う肝機能障害、黄疸があらわれることがある。
失神、意識喪失 (頻度不明)
血圧低下に伴う一過性の意識喪失等があらわれることがある。
その他の副作用
| 0.1~1%未満 | 0.1%未満 | 頻度不明 |
|---|
過敏症 | 発疹 | そう痒感、蕁麻疹 | 多形紅斑 |
|---|
精神神経系 | めまい・ふらつき、頭痛・頭重 | 倦怠感、眠気、耳鳴、しびれ感、振戦、味覚異常 | 頭がボーッとする |
|---|
循環器 | 立ちくらみ、低血圧 | 動悸、ほてり、不整脈(期外収縮、心房細動等) | 頻脈 |
|---|
消化器 | 胃部不快感、下痢 | 便秘、口渇、嘔気、嘔吐、膨満感、腹痛 | |
|---|
肝臓 | AST、ALTの上昇 | LDH、Al-Pの上昇 | |
|---|
血液 | | | 血小板数減少 |
|---|
眼 | | 霧視 | 術中虹彩緊張低下症候群(IFIS)、色視症 |
|---|
その他 | | 浮腫、尿失禁、悪寒、眼瞼浮腫、肩こり、鼻閉、勃起障害 | 女性化乳房、胸痛 |
|---|
注)発現頻度は使用成績調査を含む
適用上の注意
薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
その他の注意
臨床使用に基づく情報
類似化合物(プラゾシン塩酸塩)で腎及びその他の動脈狭窄、脚部及びその他の動脈瘤等の血管障害のある高血圧患者で、急性熱性多発性関節炎がみられたとの報告がある。
α1遮断薬を服用中又は過去に服用経験のある患者において、α1遮断作用によると考えられる術中虹彩緊張低下症候群(Intraoperative Floppy Iris Syndrome)があらわれるとの報告がある。
非臨床試験に基づく情報
動物実験(マウス)において、300mg/kg/日(臨床最大用量の約200倍)を2年間経口投与した場合、雌で乳腺腫瘍の発生頻度が対照群に比し有意に増加したとの報告がある。また、マウスに同用量を77週間経口投与した結果、血清プロラクチンが対照群に比し上昇したとの報告がある。
薬物動態
血中濃度
生物学的同等性試験
〈ナフトピジル錠75mg「トーワ」〉
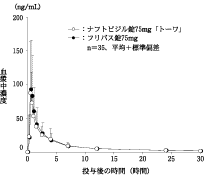
ナフトピジル錠75mg「トーワ」とフリバス錠75mgを、クロスオーバー法によりそれぞれ1錠(ナフトピジルとして75mg)健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について統計解析を行った結果、AUCについては対数値の平均値の差の90%信頼区間がlog(0.80)~log(1.25)の範囲内であり、Cmaxについては対数値の平均値の差がlog(0.90)~log(1.11)で、かつ、溶出試験で規定するすべての条件で溶出挙動が類似していることから、両剤の生物学的同等性が確認された。
| 判定パラメータ | 参考パラメータ |
AUC0-30 (ng・hr/mL) | Cmax (ng/mL) | Tmax (時間) | 半減期 (時間) |
ナフトピジル錠75mg「トーワ」 | 272.3±110.2 | 101.4±68.0 | 1.65±4.99 | 11.04±7.82※ |
フリバス錠75mg | 276.4±121.3 | 109.9±71.4 | 0.78±0.67 | 10.64±5.72 |
PharmacokineticsEtc
〈ナフトピジル錠25mg「トーワ」、ナフトピジル錠50mg「トーワ」〉
ナフトピジル錠25mg「トーワ」、ナフトピジル錠50mg「トーワ」は、ナフトピジル錠75mg「トーワ」を標準製剤としたとき、溶出挙動が同等と判断され、生物学的に同等とみなされた。,
有効成分に関する理化学的知見
一般的名称
ナフトピジル(Naftopidil)
化学名
(2RS)-1-[4-(2-Methoxyphenyl)piperazin-1-yl]-
3-(naphthalen-1-yloxy)propan-2-ol
分子式
C24H28N2O3
分子量
392.49
性状
白色の結晶性の粉末である。無水酢酸に極めて溶けやすく、N,N-ジメチルホルムアミド又は酢酸(100)に溶けやすく、メタノール又はエタノール(99.5)に溶けにくく、水にほとんど溶けない。光によって徐々に淡褐色となる。N,N-ジメチルホルムアミド溶液(1→10)は旋光性を示さない。
化学構造式
融点
126~129℃
取扱い上の注意
外箱開封後は遮光して保存すること。本剤は光により変色することがある。変色したものは使用しないこと。
包装
〈ナフトピジル錠25mg「トーワ」〉
100錠[10錠×10:PTP]
〈ナフトピジル錠50mg「トーワ」〉
100錠[10錠×10:PTP]
〈ナフトピジル錠75mg「トーワ」〉
100錠[10錠×10:PTP]
主要文献
1
社内資料:生物学的同等性試験(錠75mg)
2
社内資料:生物学的同等性試験(錠25mg)
3
社内資料:生物学的同等性試験(錠50mg)
文献請求先及び問い合わせ先
〒570-0081 大阪府守口市日吉町2丁目5番15号
製造販売業者等








 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379