1
Hansten,P.D.:Drug Intel.Clin.Pharm.1980;14:331-334
2
Northcutt,R.C.et al.:JAMA.1969;208(10):1857-1861
3
Campbell,N.R.C.et al.:Ann.Intern.Med.1992;117(12):1010-1013
4
Sherman,S.I.et al.:Am.J.Med.1994;96:531-535
5
Liel,Y.et al.:Am.J.Med.1994;97:363-365
6
Singh,N.et al.:JAMA.2000;283(21):2822-2825
7
Blackshear,J.L.et al.:Ann.Intern.Med.1983;99(3):341-342
8
仁瓶禮之他:医学のあゆみ.1978;104(2):100-102
9
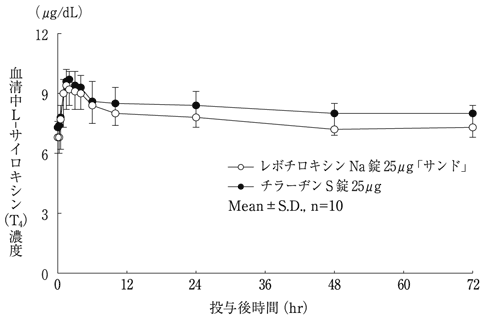
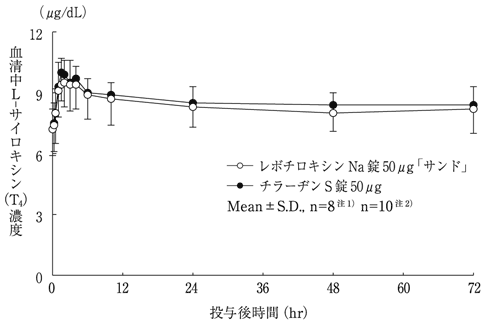
社内資料:生物学的同等性試験(レボチロキシンNa錠25μg「サンド」、同50μg「サンド」)
10
Darras,V.M.et al.:J.Endocrinol.2012;215(2):189-206
11
Wu,S.Y.et al.:Thyroid.2005;15(8):943-958
12
Yen,P.M.:Physiol.Rev.2001;81(3):1097-1142