1
永松信哉他:薬理と治療, 1997;25(6):1637-1651
2
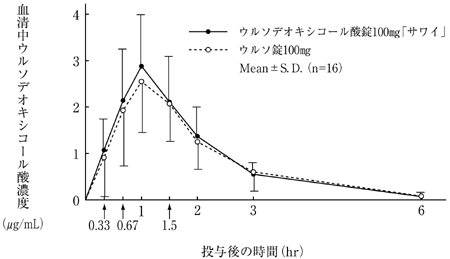
社内資料:生物学的同等性試験
3
Fedorowski, T. et al.:Gastroenterology, 1977;73(5):1131-1137
4
戸田安士他:基礎と臨床, 1976;10(1):103-119
5
宮地一馬他:臨床と研究, 1976;53(5):1395-1403
6
芦沢真六他:医学のあゆみ, 1977;101(13):922-936
7
戸田剛太郎他:肝胆膵, 1998;37(3):443-460
8
Omata, M. et al.:Gut, 2007;56(12):1747-1753
9
戸田剛太郎他:医学と薬学, 1999;41(4):609-633
10
長期投与試験(ウルソ錠:2007年3月2日承認、審査報告書)
11
吉岡正智他:診断と治療, 1976;64(10):1953-1963
12
早川富博他:日本消化器病学会雑誌, 1988;85(11):2389-2395
13
武内喜茂他:薬理と治療, 1998;26(2):169-176
14
Ishizaki, K. et al.:Eur. J. Pharmacol., 2008;578(1):57-64
15
Iwaki, T. et al.:World J. Gastroenterol., 2007;13(37):5003-5008
16
木村恒夫:日本消化器病学会雑誌, 1980;77(2):185-194
17
細胞系に対するサイトカイン・ケモカイン産生抑制作用(ウルソ錠:2007年3月2日承認、審査報告書)
18
土屋周二他:厚生省特定疾患消化吸収障害調査研究班 昭和57年度業績集, 1982;99-104
19
原泰寛他:福岡医誌, 1974;65(12):933-940
20
菅田文夫他:日本消化器病学会雑誌, 1978;75(4):492-499
21
Igimi, H. et al.:Gastroenterol. Jpn., 1983;18(2):93-97
22
堀内至:胆道, 1988;2(3):239-247
23
Crosignani, A. et al.:Hepatology, 1991;14(6):1000-1007
24
Terasaki, S. et al.:Am. J. Gastroenterol., 1991;86(9):1194-1199
25
Yoshikawa, M. et al.:Hepatology, 1992;16(2):358-364
26
Tanaka, H. et al.:J. Immunol., 1996;156(4):1601-1608