1
三好秋馬 他:内科宝函.1977;24(4):105-115
2
橋爪武司 他:応用薬理.1976;12(5):691-702
3
川野 淳 他:診療と新薬.1982;19(1):27-32
4
宮本二郎 他:Prog. Med.1982;2(6):922-928
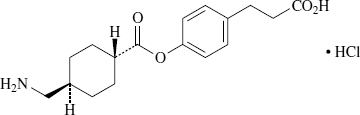
粘膜防御性 胃炎・胃潰瘍治療剤
1g 17.5円
有効成分 | 1カプセル中 セトラキサート塩酸塩(日局) 200mg |
|---|---|
添加剤 | トウモロコシデンプン、ステアリン酸マグネシウム、タルク カプセル:ゼラチン、マクロゴール4000、酸化チタン、ラウリル硫酸ナトリウム、青色1号 |
有効成分 | 1g中 セトラキサート塩酸塩(日局) 400mg |
|---|---|
添加剤 | トウモロコシデンプン、タルク、マクロゴール6000、軽質無水ケイ酸、トコフェロール、メタクリル酸コポリマーS、アスパルテーム(L-フェニルアラニン化合物)、メタケイ酸アルミン酸マグネシウム、香料 |
| 外形 |  |
|---|---|
| 大きさ | 大きさ(直径) 17.8mm |
| 質量 | 315mg |
| 識別コード |  |
| 色・剤形 | キャップ:青色不透明、ボディー:白色不透明・カプセル(2号) |
| 色・剤形 | 白色~微黄色・コーティング細粒 |
|---|
0.1~1%未満 | 頻度不明 | |
|---|---|---|
消化器 | 口渇、悪心・嘔吐、下痢、便秘、胃部不快感・膨満感 | - |
過敏症 | 発疹、そう痒感 | - |
その他 | - | AST上昇、ALT上昇等 |
改善率(%)〔改善例/総症例〕 | |
200mg/日投与群 | 63.1〔70/111〕 |
800mg/日投与群 | 73.8〔79/107〕 |
改善率(%)〔改善例/総症例〕 | |||
1週 | 2週 | 4週 | |
本剤投与群 | 82.1〔23/28〕 | 75.9〔41/54〕 | 73.1〔57/78〕 |
アルジオキサ投与群 | 68.4〔13/19〕 | 85.0〔34/40〕 | 77.6〔45/58〕 |
治癒率(%)〔治癒例/総症例〕 | |
本剤投与群 | 88.6〔39/44〕注) |
プラセボ投与群 | 62.2〔28/45〕注) |
治癒率(%)〔治癒例/総症例〕 | |||
4週 | 8週注) | 12週注) | |
本剤投与群 | 28.2〔31/110〕 | 60.9〔67/110〕 | 72.7〔80/110〕 |
ゲファルナート投与群 | 23.3〔27/116〕 | 46.6〔54/116〕 | 55.2〔64/116〕 |
治癒率(%)〔治癒例/総症例〕 | |
本剤単独 | 70.1〔384/548〕 |
他剤併用 (抗コリン薬、制酸薬、抗潰瘍薬) | 79.9〔131/164〕 |