1
Mukwaya, G. et al.:Antimicrob. Agents Chemother., 2005;49:4903-4910
2
Sadeque, A. J. M. et al.:Clin. Pharmacol. Ther., 2000;68:231-237
3
Niemi, M. et al.:Eur. J. Clin. Pharmacol., 2006;62:463-472
4
Callréus, T. et al.:Eur. J. Clin. Pharmacol., 1999;55:305-309
5
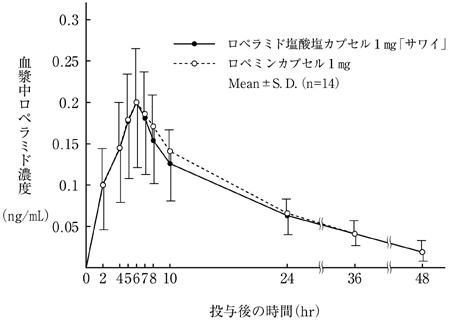
社内資料:生物学的同等性試験
6
荘司行伸他:日本薬理学雑誌, 1978;74:145-154