1
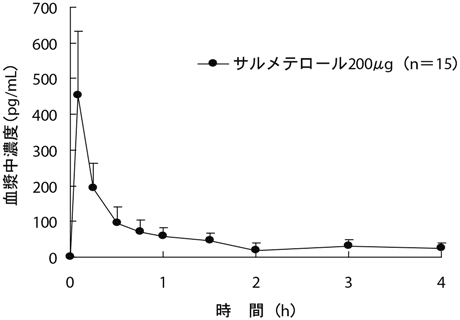
江角凱夫ほか:基礎と臨床.1993;27:4211-4230
2
Nelson HS,et al.:Chest.2006;129:15-26
3
Manchee GR,et al.:Drug Metab Dispos.1993;21:1022-1028
4
牧野荘平:臨床医薬.2002;18:791-805
5
宮本昭正ほか:臨床医薬.1993(2002年改訂);9(Suppl.4):49-79
6
宮本昭正ほか:臨床医薬.1993(2002年改訂);9(Suppl.4):81-111
7
宮本昭正ほか:臨床医薬.2002;18:411-436
8
宮本昭正ほか:臨床医薬.2002;18:461-483
9
湯川龍雄ほか:臨床医薬.1993(2002年改訂);9(Suppl.4):113-131
10
中野均ほか:臨床医薬.2002;18:807-819
11
宮本昭正ほか:臨床医薬.2002;18:437-459
12
東田有智ほか:アレルギー・免疫.2006;13:1154-1170
13
福地義之助ほか:呼吸.2006;25:186-199
14
武田憲三ほか:基礎と臨床.1994;28:1361-1379
15
宮本昭正ほか:臨床医薬.1993(2002年改訂);9(Suppl.4):23-48
16
宮本昭正ほか:臨床医薬.1993(2002年改訂);9(Suppl.4):219-241
17
川合満ほか:臨床医薬.2003;19:497-506
18
相良博典ほか:臨床医薬.1993;9:2701-2709
19
Whelan CJ,et al.:Br J Pharmacol.1993;110:613-618
20
Yamamura H,et al.:Jpn J Allergol.1991;40:669-679
21
Butchers PR,et al.:Br J Pharmacol.1991;104:672-676
22
甲斐広文ほか:応用薬理.1993;45:119-124
23
佐野靖之ほか:臨床医薬.2002;18:705-717