1
社内資料:生物学的同等性試験
2
長岡 滋ほか.:薬理と治療.1981;9(5):1845-1854.
3
千田勝一ほか.:薬理と治療.1981;9(2):483-486.
4
前多治雄ほか.:薬理と治療.1981;9(2):487-490.
5
Curti PC.:Pneumonologie.1972;147(1):62-74.
6
Curti PC,et al.:Arzneim-Forsch.1978;28(5a):922-925.
気道潤滑去痰剤
1mL 5.2円
有効成分 | 1mL中 |
|---|---|
有効成分 | アンブロキソール塩酸塩… 3mg |
添加剤 | D-ソルビトール液、グリセリン、パラオキシ安息香酸メチル、パラオキシ安息香酸エチル、リン酸二水素ナトリウム、pH調節剤(塩酸、水酸化ナトリウム)、香料 |
| 剤形 | 液で、芳香があり、味は甘い。 |
|---|---|
| 色調 | 無色~微黄色澄明 |
| pH | 3.5~4.5 |
0.1~5%未満 | 0.1%未満 | 頻度不明 | |
|---|---|---|---|
消化器 | 胃不快感 | 胃痛、腹部膨満感、腹痛、下痢、嘔気、嘔吐、便秘、食思不振、消化不良(胃部膨満感、胸やけ等) | |
過敏症 | 発疹、蕁麻疹、蕁麻疹様紅斑、そう痒 | 血管浮腫(顔面浮腫、眼瞼浮腫、口唇浮腫等) | |
肝臓 | 肝機能障害(AST上昇、ALT上昇等) | ||
その他 | 口内しびれ感、上肢のしびれ感 | めまい |
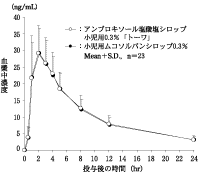
製剤投与量 (アンブロキソール 塩酸塩として) | 判定パラメータ | 参考パラメータ | |||
AUC0-24 (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | ||
アンブロキソール塩酸塩 シロップ小児用0.3%「トーワ」 | 5mL (15mg) | 259.9±78.9 | 30.33±9.38 | 1.87±0.46 | 8.10±0.77 |
小児用ムコソルバン シロップ0.3% | 5mL (15mg) | 254.5±69.8 | 29.87±7.38 | 1.91±0.51 | 8.20±0.99 |
 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379