1
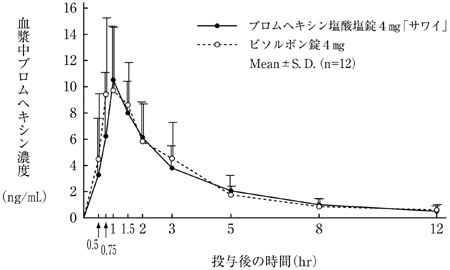
社内資料:生物学的同等性試験
2
Kopitar, Z. et al.:Arzneimittelforschung, 1971;21:914-918
3
Jauch, R. et al.:Arzneimittelforschung, 1975;25:1954-1958
4
第十八改正日本薬局方解説書, 廣川書店, 2021;C-5118-5122
5
Engelhorn, R. et al.:Arzneimittelforschung, 1963;13:474-480
6
原田康夫他:耳鼻臨床, 1976;69:553-562
7
Bruce, R. A. et al.:Br. J. Clin. Pract., 1968;22:289-292
8
Takeda, H. et al.:Jpn. J. Pharmacol., 1983;33:455-461
9
Gil, J. et al.:Respiration, 1971;28:438-456
10
Wichert, P. V. et al.:Pneumonologie, 1971;144:323-327
11
Yanaura, S. et al.:Jpn. J. Pharmacol., 1981;31:957-965