1
Zurth C, et al.:Eur J Drug Metab Pharmacokinet. 2019;44(6):747-59
2
単回投与後の血漿中濃度, 1996(クレストール錠:2005年1月19日承認、申請資料概要へ3.3.1.2)
3
Martin PD, et al. Clin Ther 2003;25(8):2215-24
4
反復投与後の血漿中濃度, 2001(クレストール錠:2005年1月19日承認、申請資料概要へ3.4)
5
反復投与後の血中濃度(クレストール錠:2005年1月19日承認、申請資料概要イ3.2.2.2)
6
患者における血漿中濃度, 2002(クレストール錠:2005年1月19日承認、申請資料概要へ3.6)
7
患者における血漿中濃度(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.8)
8
Martin PD, et al. Br J Clin Pharmacol. 2002;54(5):472-7
9
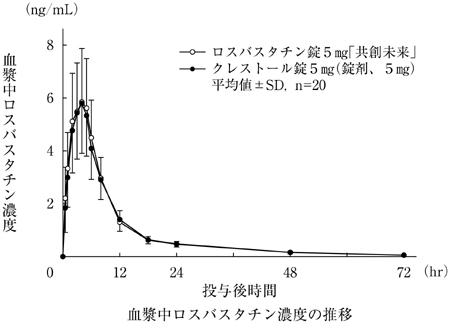
共創未来ファーマ株式会社 社内資料:ロスバスタチン錠5mg「共創未来」の生物学的同等性試験に関する資料(2016)
10
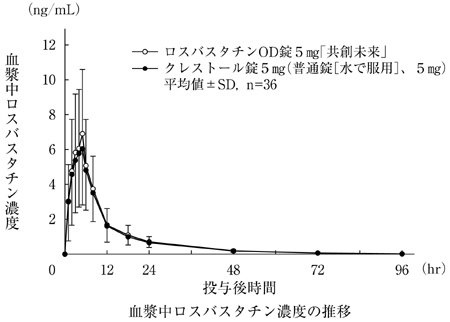
共創未来ファーマ株式会社 社内資料:ロスバスタチンOD錠5mg「共創未来」の生物学的同等性試験(水なし)に関する資料(2017)
11
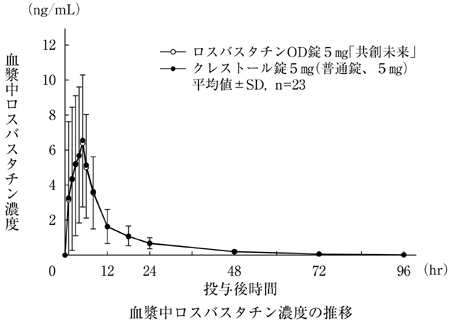
共創未来ファーマ株式会社 社内資料:ロスバスタチンOD錠5mg「共創未来」の生物学的同等性試験(水あり)に関する資料(2016)
12
生物学的利用率, 2001(クレストール錠:2005年1月19日承認、申請資料概要へ3.5)
13
食事の影響, 2000(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.5)
14
蛋白結合率, 2000(クレストール錠:2005年1月19日承認、申請資料概要へ2.2.5)
15
尿糞中排泄率, 1999(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.9.5)
16
HMG-CoA還元酵素阻害活性体の血漿中濃度, 2000(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.9.4)
17
Martin PD, et al. J Clin Pharmacol. 2002;42(10):1116-21
18
Simonson SG, et al. Eur J Clin Pharmacol. 2003;58(10):669-75
19
腎障害の影響, 2001(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.11)
20
薬物相互作用-制酸剤, 2000(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.12.2(f))
21
Simonson SG, et al. Clin Pharmacol Ther. 2004;76(2):167-77
22
Schneck DW, et al. Clin Pharmacol Ther. 2004;75(5):455-63
23
Cooper KJ, et al. Eur J Clin Pharmacol. 2002;58(8):527-31
24
Cooper KJ, et al. Br J Clin Pharmacol. 2003;55(1):94-9
25
Cooper KJ, et al. Clin Pharmacol Ther. 2003;73(4):322-9
26
Cooper KJ, et al. Eur J Clin Pharmacol. 2003;59(1):51-6
27
Simonson SG, et al. J Clin Pharmacol. 2005;45(8):927-34
28
Martin PD, et al. J Clin Pharmacol. 2002;42(12):1352-7
29
Simonson SG, et al. Br J Clin Pharmacol. 2004;57(3):279-86
30
McCormick AD, et al. J Clin Pharmacol. 2000;40:1055
31
ロスバスタチンのin vitro代謝(クレストール錠:2005年1月19日承認、申請資料概要へ3.7.9)
32
共創未来ファーマ株式会社 社内資料:ロスバスタチン錠2.5mg「共創未来」の溶出試験に関する資料(2016)
33
共創未来ファーマ株式会社 社内資料:ロスバスタチンOD錠2.5mg「共創未来」の溶出試験に関する資料(2016)
34
Schneck DW, et al. Am J Cardiol. 2003;91(1):33-41
35
アトルバスタチンとの用量反応比較試験(クレストール錠:2005年1月19日承認、申請資料概要ト1.3.2)
36
日本人高コレステロール血症患者における有効性, 2002(クレストール錠:2005年1月19日承認、申請資料概要ト1.2.3)
37
外国人高コレステロール血症患者における有効性, 2001(クレストール錠:2005年1月19日承認、申請資料概要ト2.1.2.1)
38
外国人高コレステロール血症患者の長期投与における有効性, 2001(クレストール錠:2005年1月19日承認、申請資料概要ト1.5.2)
39
Olsson AG, et al. Am Heart J. 2002;144(6):1044-51
40
Mabuchi H, et al. J Atheroscler Thromb. 2004;11(3):152-8
41
ヘテロ接合体性FH患者における増量、長期投与試験(クレストール錠:2005年1月19日承認、申請資料概要ト1.4.2)
42
Nezasa K, et al. Xenobiotica. 2003;33(4):379-88
43
作用機序のまとめ(クレストール錠:2005年1月19日承認、申請資料概要ホ1.2.8)
44
McTaggart F, et al. Am J Cardiol. 2001;87(5A):28B-32B
45
LDL受容体に対する作用, 2002(クレストール錠:2005年1月19日承認、申請資料概要ホ1.2.3)
46
イヌの血中脂質に対する作用, 2002(クレストール錠:2005年1月19日承認、申請資料概要ホ1.1.1)
47
カニクイザルの血清コレステロール及びリポ蛋白コレステロールに対する作用, 2002(クレストール錠:2005年1月19日承認、申請資料概要ホ1.1.2)
48
WHHLウサギの血清コレステロール及び動脈硬化病変に対する作用, 2002(クレストール錠:2005年1月19日承認、申請資料概要ホ1.1.3)
49
アポ蛋白E*3Leidenトランスジェニックマウスに対する作用, 2002(クレストール錠:2005年1月19日承認、申請資料概要ホ1.1.4)
50
ヒトアポ蛋白B/CETPトランスジェニックマウスに対する作用, 2002(クレストール錠:2005年1月19日承認、申請資料概要ホ1.1.5)