1
Vaidyanathan, S. et al.:Cardiovasc. Ther. 2008;26(4):238-246
2
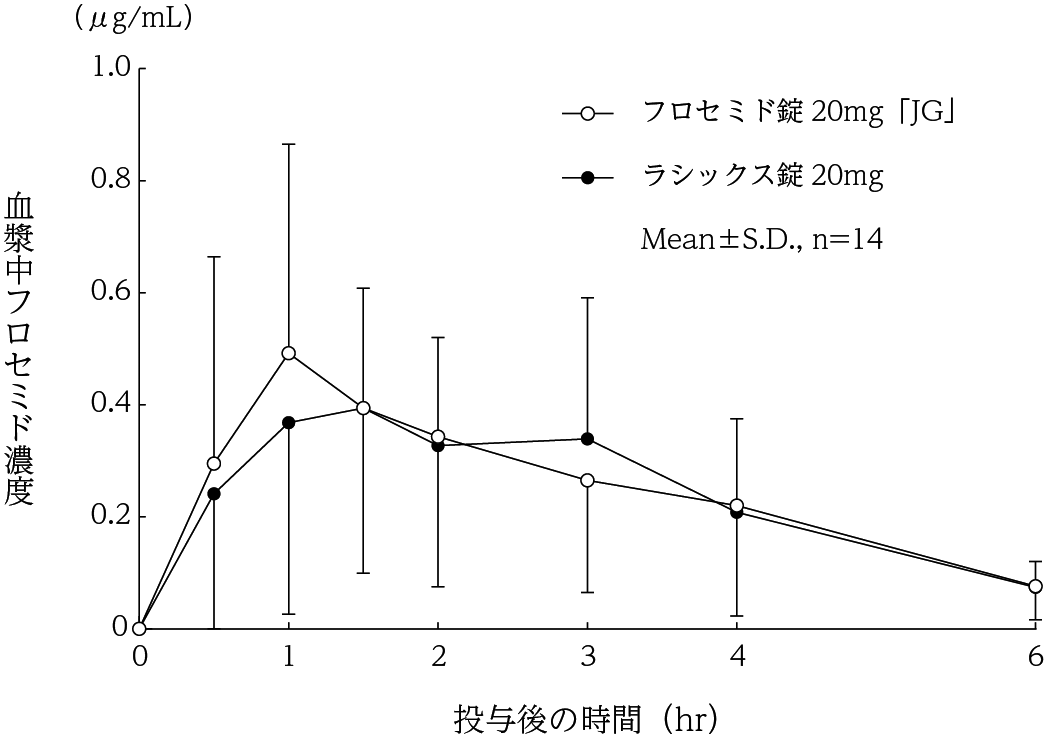
社内資料:生物学的同等性試験(錠20mg)
3
Cutler, R.E. et al.:Clin. Pharmacokin. 1979;4(4):279-296
4
Hammarlund-Udenaes, M. et al.:J. Pharmacokin. Biopharm. 1989;17(1):1-46
5
Suzuki, F. et al.:Klin. Wschr. 1964;42(12):569-571
6
Rupp, W. et al.:Symposion in Schloß Reinhartshausen am Rhein. 1969;12 Mai
7
Timmerman, R.J. et al.:Curr. Ther. Res. 1964;6(2):88-94
8
Vorburger, C.:J. Urol. Nephrol. 1966;72(9):581-590
9
Häussler, A. et al.:Arzneim.-Forsch. 1964;14(6):710-713
10
Muth, R.G.:Ann. Intern. Med. 1968;69(2):249-261
11
Heimsoth, V.H.:Münch. med. Wschr. 1975;117(28):1199-1204