作成又は改訂年月
日本標準商品分類番号
薬効分類名
承認等
販売名
メキシレチン塩酸塩カプセル50mg「日医工」
販売名コード
承認・許可番号
22500AMX00440000
Mexiletine Hydrochloride
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存,遮光保存
使用期限
外箱等に表示の使用期限内に使用すること
規制区分
劇薬
処方せん医薬品
(注意−医師等の処方せんにより使用すること)
組成
メキシレチン塩酸塩カプセル50mg「日医工」
1カプセル中メキシレチン塩酸塩50mgを含有する。
添加物としてトウモロコシデンプン,セルロース,無水ケイ酸,ステアリン酸マグネシウムを含有する。また,カプセル本体にゼラチン,タルク,ラウリル硫酸ナトリウム,酸化チタン,黄色三二酸化鉄,赤色3号を含有する。
製剤の性状
| 薄い黄赤色(キャップ)/薄い黄褐色(ボディ)の硬カプセル剤である。 |
| 号数 | 外形 | 本体コード | 包装コード |
| 4 |  |  751/50 751/50 |  751 751 |
販売名
メキシレチン塩酸塩カプセル100mg「日医工」
販売名コード
承認・許可番号
22500AMX00441000
Mexiletine Hydrochloride
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
室温保存,遮光保存
使用期限
外箱等に表示の使用期限内に使用すること
規制区分
劇薬
処方せん医薬品
(注意−医師等の処方せんにより使用すること)
組成
メキシレチン塩酸塩カプセル100mg「日医工」
1カプセル中メキシレチン塩酸塩100mgを含有する。
添加物としてトウモロコシデンプン,セルロース,無水ケイ酸,ステアリン酸マグネシウムを含有する。また,カプセル本体にゼラチン,タルク,ラウリル硫酸ナトリウム,酸化チタン,黄色三二酸化鉄,赤色3号を含有する。
製剤の性状
| 薄い黄赤色(キャップ)/白色(ボディ)の硬カプセル剤である。 |
| 号数 | 外形 | 本体コード | 包装コード |
| 2 |  |  752/100 752/100 |  752 752 |
一般的名称
禁忌
本剤の成分に対し過敏症の既往歴のある患者
重篤な刺激伝導障害(ペースメーカー未使用のII〜III度房室ブロック等)のある患者[刺激伝導障害の悪化,心停止を来すことがある。]
原則禁忌
糖尿病性神経障害に伴う自覚症状(自発痛,しびれ感)の改善を目的として投与する場合:
重篤な心不全を合併している患者[心不全を合併している糖尿病性神経障害患者に対する安全性は確立していない(使用経験がない)ので,重篤な心不全を合併している患者には,自覚症状(自発痛,しびれ感)に対する本剤の有益性が危険性(心不全の悪化,不整脈の誘発等)を上回ると判断される場合にのみ投与すること。]
効能又は効果
頻脈性不整脈(心室性)
糖尿病性神経障害に伴う自覚症状(自発痛,しびれ感)の改善
用法及び用量
頻脈性不整脈(心室性)
通常,成人にはメキシレチン塩酸塩として,1日300mgより投与をはじめ,効果が不十分な場合は450mgまで増量し,1日3回に分割し食後に経口投与する。
なお,年齢,症状により適宜増減する。
糖尿病性神経障害に伴う自覚症状(自発痛,しびれ感)の改善
通常,成人にはメキシレチン塩酸塩として,1日300mgを1日3回に分割し食後に経口投与する。
用法及び用量に関連する使用上の注意
頻脈性不整脈(心室性)に投与する場合:
1日用量450mgを超えて投与する場合,副作用発現の可能性が増大するので注意すること。(「過量投与」の項参照)
糖尿病性神経障害に伴う自覚症状(自発痛,しびれ感)の改善を目的として投与する場合:
2週間投与しても効果が認められない場合には,投与を中止すること。(「重要な基本的注意」の項参照)
1日300mgの用量を超えて投与しないこと。(「重要な基本的注意」の項参照)
使用上の注意
慎重投与
基礎心疾患(心筋梗塞,弁膜症,心筋症等)のある患者[心機能抑制や催不整脈作用が出現することがある。]
軽度の刺激伝導障害(不完全房室ブロック,脚ブロック等)のある患者[刺激伝導障害を悪化させることがある。]
著明な洞性徐脈のある患者[徐脈を悪化させることがある。]
重篤な肝・腎障害のある患者[本剤の血中濃度が上昇することがある。]
心不全のある患者[心不全を悪化,不整脈を悪化・誘発させることがあり,また,本剤の血中濃度が上昇することがある。]
低血圧の患者[循環状態を悪化させることがある。]
パーキンソン症候群の患者[振戦を増強させることがある。]
高齢者(「重要な基本的注意」及び「高齢者への投与」の項参照)
血清カリウム低下のある患者[不整脈を誘発させることがある。]
他の抗不整脈薬による治療を受けている患者[有効性,安全性が確立していない。(「重要な基本的注意」及び「相互作用」の項参照)]
重要な基本的注意
本剤の投与に際しては,頻回に患者の状態を観察し,心電図,脈拍,血圧,心胸比を定期的に調べること。PQの延長,QRS幅の増大,QTの延長,徐脈,血圧低下等の異常所見が認められた場合には,直ちに減量又は投与を中止すること。
特に,次の患者又は場合には,少量から開始するなど投与量に十分注意するとともに,頻回に心電図検査を実施すること。
心不全のある患者又は基礎心疾患(心筋梗塞,弁膜症,心筋症等)があり,心不全を来すおそれのある患者(心室頻拍,心室細動等が発現するおそれが高いので,開始後1〜2週間は入院させること。)
高齢者(入院させて開始することが望ましい。「高齢者への投与」の項参照)
他の抗不整脈薬との併用(有効性,安全性が確立していない。)
紅斑,水疱・びらん,結膜炎,口内炎,発熱等があらわれた場合には中毒性表皮壊死症(Lyell症候群),皮膚粘膜眼症候群(Stevens‐Johnson症候群),紅皮症の前駆症状である可能性があるため,投与を中止し,直ちに皮膚科専門医を受診させるなど適切な処置を行うこと。
頭がボーとする,めまい,しびれ等の精神神経系症状が発現し,増悪する傾向がある場合には,直ちに減量又は投与を中止すること。また,本剤投与中の患者には自動車の運転等危険を伴う機械の操作に従事させないよう注意すること。
他の抗不整脈薬(リン酸ジソピラミド)でテルフェナジンとの併用により,QT延長,心室性不整脈を起こしたとの報告がある。
本剤は心臓ペーシング閾値を上昇させる場合があるので,恒久的ペースメーカー使用中,あるいは一時的ペーシング中の患者に対しては十分注意して投与すること。また,ペースメーカー使用中の患者に投与する場合は適当な間隔でペーシング閾値を測定すること。異常が認められた場合には直ちに減量又は投与を中止すること。
また,本剤は植え込み型除細動器(ICD)の除細動閾値を上昇させる場合があるので,ICDを使用している患者に本剤を追加投与した場合又は本剤の投与量の変更を行った場合には,十分に注意して経過観察を行うこと。
糖尿病性神経障害の患者に投与する場合
本剤による治療は原因療法ではなく対症療法であるので,漫然と投与しないこと。
糖尿病性神経障害の患者に対し1日300mgを超える投与での安全性は確立していない。(使用経験が少ない。)
2週間投与しても症状の改善が認められない場合は投与を中止し,血糖コントロールや食事療法等の適切な治療を継続すること。
糖尿病性神経障害の患者では,下肢の状態を十分に観察すること。(本剤の投与により疼痛が緩解され,末梢血管障害性の下肢の潰瘍や壊疽の進行を看過するおそれがある。)
相互作用
本剤は,主として薬物代謝酵素CYP1A2及びCYP2D6で代謝される。
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
リドカイン
プロカインアミド
キニジン
アプリンジン
カルシウム拮抗剤
β受容体遮断剤 | 本剤の作用が増強することがある。 | 両剤の陰性変力作用と変伝導作用が相加的又は相乗的に増強することがある。 |
| アミオダロン | torsades de pointesを発現したとの報告がある。 | 機序不明 |
胃排出能を抑制する薬剤
モルヒネ等 | 本剤の吸収が遅延することがある。 | モルヒネ等により胃の運動が低下し,胃内容排出時間が延長すると,本剤の吸収が遅延することがある。 |
| 肝薬物代謝酵素機能(特にチトクロームP-450系のCYP1A2及び2D6)に影響を与える薬剤 | 本剤の血中濃度に影響を与えるおそれがある。 | チトクロームP‐450(CYP1A2,2D6)による本剤の代謝が影響を受けるおそれがある。 |
| シメチジン | 本剤の血中濃度が上昇することがある。 | シメチジンによりチトクロームP‐450の薬物代謝が阻害され本剤の血中濃度が上昇することがある。 |
リファンピシン
フェニトイン | 本剤の血中濃度が低下することがある。 | 本剤の代謝が促進されることがある。 |
| テオフィリン | テオフィリンの血中濃度が上昇することがある。 | 本剤はテオフィリンに比べ,チトクロームP‐450への親和性が強く,テオフィリンの代謝が抑制される。 |
尿のpHをアルカリ化させる薬剤
炭酸水素ナトリウム等 | 本剤の血中濃度が上昇することがある。 | アルカリ性尿は,本剤の腎排泄を抑制する。 |
尿のpHを酸性化させる薬剤
塩化アンモニウム等 | 本剤の血中濃度が低下することがある。 | 酸性尿は,本剤の腎排泄を促進する。 |
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
中毒性表皮壊死症(Lyell症候群),皮膚粘膜眼症候群(Stevens‐Johnson症候群),紅皮症(頻度不明)
中毒性表皮壊死症,皮膚粘膜眼症候群,紅皮症があらわれることがあるので,観察を十分に行い,紅斑,水疱・びらん,結膜炎,口内炎,発熱等があらわれた場合には,中毒性表皮壊死症,皮膚粘膜眼症候群,紅皮症の前駆症状である可能性があるため,投与を中止し,適切な処置を行うこと。
過敏症症候群(頻度不明)
初期症状として発疹,発熱がみられ,さらにリンパ節腫脹,肝機能障害,白血球増加,好酸球増多,異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがあるので,観察を十分に行い,このような症状があらわれた場合には,投与を中止し,適切な処置を行うこと。なお,発疹,発熱,肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること。
また,過敏症症候群に伴い,1型糖尿病を発症しケトアシドーシスに至った例も報告されているので,このような場合には,適切な処置を行うこと。
心室頻拍,房室ブロック(頻度不明)
心室頻拍(torsades de pointesを含む),房室ブロックがあらわれることがあるので,観察を十分に行い,異常が認められた場合には,投与を中止するなど,適切な処置を行うこと。
腎不全(頻度不明)
腎不全があらわれることがあるので,観察を十分に行い,異常が認められた場合には,投与を中止し,適切な処置を行うこと。
幻覚,錯乱(頻度不明)
幻覚,錯乱があらわれることがあるので,観察を十分に行い,異常が認められた場合には,投与を中止し,適切な処置を行うこと。
肝機能障害,黄疸(頻度不明)
AST(GOT),ALT(GPT),γ-GTPの上昇等を伴う肝機能障害,黄疸があらわれることがあるので,観察を十分に行い,異常が認められた場合には,投与を中止し,適切な処置を行うこと。
間質性肺炎,好酸球性肺炎(頻度不明)
間質性肺炎,好酸球性肺炎があらわれることがあるので,観察を十分に行い,異常が認められた場合には,投与を中止し,副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
重大な副作用(類薬)
心停止,心室細動,失神,洞房ブロック,徐脈
本剤と類似のNaチャネル阻害作用を有する薬剤でこのような症状があらわれることがあるので,定期的かつ必要に応じて心電図検査を実施し,異常が観察された場合には,投与を中止し,適切な処置を行うこと。
その他の副作用
以下のような副作用があらわれた場合には,症状に応じて適切な処置を行うこと。
| | 頻度不明 |
| 循環器 | 動悸,徐脈,起立時めまい,QRS延長,血圧上昇,浮腫,胸部圧迫感,心房細動,低血圧 |
| 消化器 | 悪心・嘔吐,食欲不振,胸やけ,胃・腹部不快感,口渇,便秘,下痢,腹部膨満感,消化不良,腹痛,嚥下障害,口唇炎,舌炎,胃痛,食道炎,食道潰瘍 |
| 精神神経系 | 振戦,めまい,しびれ感,眠気,頭痛,不眠,耳鳴,眼振,いらいら感,複視,発汗,意識障害,痙攣,譫妄,構音障害 |
| 過敏症注1) | そう痒感,全身発疹,発熱,蕁麻疹,紅斑,多形(滲出性)紅斑 |
| 肝臓 | 尿ウロビリノゲン上昇 |
| 腎臓 | BUN上昇,クレアチニン上昇,腎機能障害 |
| 血液注2) | 白血球数異常,赤血球減少,血色素量減少,ヘマトクリット減少,血小板数異常,好酸球増多,リンパ球減少,好中球増多,顆粒球減少 |
| 泌尿器 | 排尿困難・尿閉,尿失禁 |
| その他 | 咽頭異和感,にがみ,倦怠感,咳,足のこわばり,血清カリウム上昇,総コレステロール上昇,脱力感,ほてり,味覚異常 |
注1:このような症状があらわれた場合には,投与を中止すること。
注2:観察を十分に行い,異常が認められた場合には,投与を中止すること。
高齢者への投与
高齢者では,肝・腎機能が低下していることが多く,また,体重が少ない傾向があるなど副作用が発現しやすいので,慎重に投与すること。(「重要な基本的注意」の項参照)
妊婦,産婦,授乳婦等への投与
妊婦又は妊娠している可能性のある婦人には,治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[妊娠中の投与に関する安全性は確立していない。]
授乳中の婦人に投与することを避け,やむを得ず投与する場合には授乳を中止させること。[母乳中へ移行することが報告されている。]
小児等への投与
低出生体重児,新生児,乳児,幼児又は小児に対する安全性は確立していない。
過量投与
症状
過量服用の結果,副作用の項に記載した悪心,眠気,徐脈,低血圧,痙攣,錯乱等の症状の他に,知覚異常及び心停止があらわれたとの報告があるので注意すること。また,症状に応じて適切な処置を行うこと。
処置方法
一般的な対症療法が望ましいが,過量服用の可能性のある場合は必要に応じて胃洗浄を行うこと。
徐脈,低血圧が重篤な場合,必要に応じてアトロピンを使用するなど適切な処置を行うこと。
痙攣等があらわれた場合には,直ちに投与を中止し,ベンゾジアゼピン系薬剤等の投与,人工呼吸,酸素吸入等必要に応じて適切な処置を行うこと。
適用上の注意
薬剤交付時
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により,硬い鋭角部が食道粘膜へ刺入し,更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている。)
服用時
食道に停留し,崩壊すると食道潰瘍を起こすことがあるので,多めの水で服用させ,特に就寝直前の服用等には注意すること。
その他の注意
本剤とリドカインとの交叉過敏性(交叉アレルギー)についての証明はされていないが,本剤の投与により発現した副作用症状(過敏症状等)が,本剤の投与中止後,リドカイン投与により再発したとの報告がある。
薬物動態
生物学的同等性試験
メキシレチン塩酸塩カプセル50mg「日医工」及び標準製剤を,クロスオーバー法によりそれぞれ1カプセル(メキシレチン塩酸塩として50mg)健康成人男子に絶食単回経口投与して血清中メキシレチン濃度を測定し,得られた薬物動態パラメータ(AUC,Cmax)について統計解析を行った結果,両剤の生物学的同等性が確認された。
1)また,メキシレチン塩酸塩カプセル100mg「日医工」及び標準製剤をそれぞれ1カプセル(メキシレチン塩酸塩として100mg)経口投与した場合においても,同様に両剤の生物学的同等性が確認された。
1)(注意:本剤の承認された用法は食後投与である。)
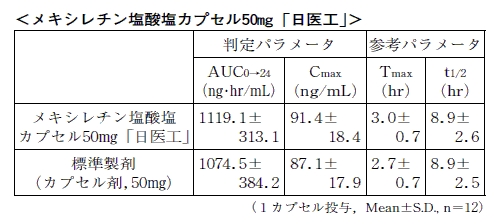
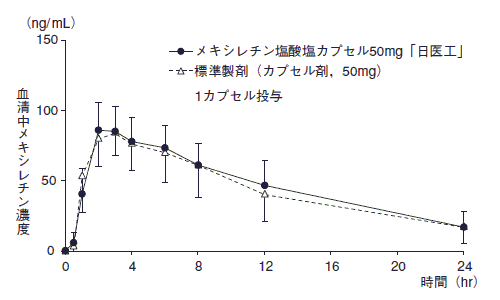
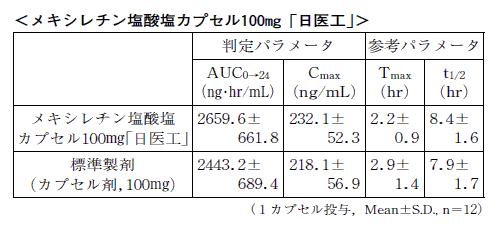
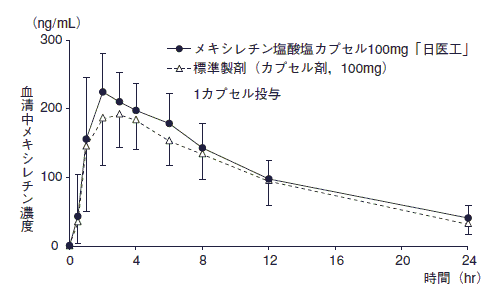
血清中濃度並びにAUC,Cmax等のパラメータは,被験者の選択,体液の採取回数・時間等の試験条件によって異なる可能性がある。
溶出挙動
メキシレチン塩酸塩カプセル50mg「日医工」及びメキシレチン塩酸塩カプセル100mg「日医工」は,日本薬局方外医薬品規格第3部に定められたメキシレチン塩酸塩カプセルの溶出規格に適合していることが確認されている。2)
有効成分に関する理化学的知見
一般名
メキシレチン塩酸塩(Mexiletine Hydrochloride)
化学名
(1
RS)-2-(2,6-Dimethylphenoxy)-1-methylethylamine monohydrochloride
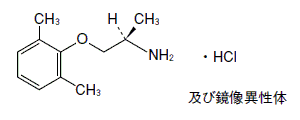
分子式
C11H17NO・HCl
分子量
215.72
性状
白色の粉末である。
水又はエタノール(95)に溶けやすく,アセトニトリルに溶けにくく,ジエチルエーテルにほとんど溶けない。
本品の水溶液(1→20)は旋光性を示さない。
本品1.0gを水10mLに溶かした液のpHは3.8〜5.8である。
融点
200〜204℃
取扱い上の注意
安定性試験
本品につき加速試験(40℃,相対湿度75%,6ヵ月)を行った結果,メキシレチン塩酸塩カプセル50mg「日医工」及びメキシレチン塩酸塩カプセル100mg「日医工」は通常の市場流通下において3年間安定であることが推測された。3)
包装
メキシレチン塩酸塩カプセル50mg「日医工」
100カプセル(10カプセル×10;PTP)
1000カプセル(10カプセル×100;PTP)
250カプセル(バラ)
メキシレチン塩酸塩カプセル100mg「日医工」
100カプセル(10カプセル×10;PTP)
1000カプセル(10カプセル×100;PTP)
250カプセル(バラ)
主要文献及び文献請求先
主要文献
1
日医工株式会社 社内資料:生物学的同等性試験
2
日医工株式会社 社内資料:溶出試験
3
日医工株式会社 社内資料:安定性試験
文献請求先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
日医工株式会社 お客様サポートセンター
〒930‐8583 富山市総曲輪1丁目6番21
フリーダイアル(0120)517-215
Fax(076)442-8948
製造販売業者等の氏名又は名称及び住所
製造販売元
日医工株式会社
富山市総曲輪1丁目6番21
 751/50
751/50 751
751
 752/100
752/100 752
752



