添付文書番号
1319816Q1042_1_03
企業コード
380003
作成又は改訂年月
日本標準商品分類番号
871319
薬効分類名
眼科手術補助剤
承認等
販売名
シェルガン0.5眼粘弾剤
販売名コード
販売名英字表記
SHELLGAN 0.5 Ophthalmic Viscoelastic Preparation
販売名ひらがな
しぇるがん0.5がんねんだんざい
承認番号等
販売開始年月
貯法、有効期間
一般的名称
精製ヒアルロン酸ナトリウム/コンドロイチン硫酸エステルナトリウム
組成・性状
組成
シェルガン0.5眼粘弾剤
有効成分 | 1筒(0.5mL)中
日局 精製ヒアルロン酸ナトリウム 15mg |
|---|
有効成分 | 1筒(0.5mL)中
コンドロイチン硫酸エステルナトリウム 20mg |
|---|
添加剤 | 塩化ナトリウム、リン酸二水素ナトリウム水和物、リン酸水素ナトリウム水和物、D-ソルビトール |
|---|
製剤の性状
シェルガン0.5眼粘弾剤
| 剤形 | プレフィルドシリンジ製剤 |
|---|
| pH | 7.0~7.5 |
|---|
| 浸透圧比 | 0.9~1.3(生理食塩液に対する比) |
|---|
| 性状 | 無色澄明の粘稠な液 |
|---|
| 粘度 | 35000~60000mPa・s(25℃、せん断速度 2s-1) |
|---|
効能又は効果
次の一連の眼科手術における手術補助:
超音波乳化吸引法による白内障摘出術及び眼内レンズ挿入術
用法及び用量
通常、超音波乳化吸引法による白内障摘出時には0.1~0.4mL、眼内レンズ挿入時には0.1~0.3mLを前房内へ注入する。
又、必要に応じて眼内レンズのコーティングに0.1mL使用する。
重要な基本的注意
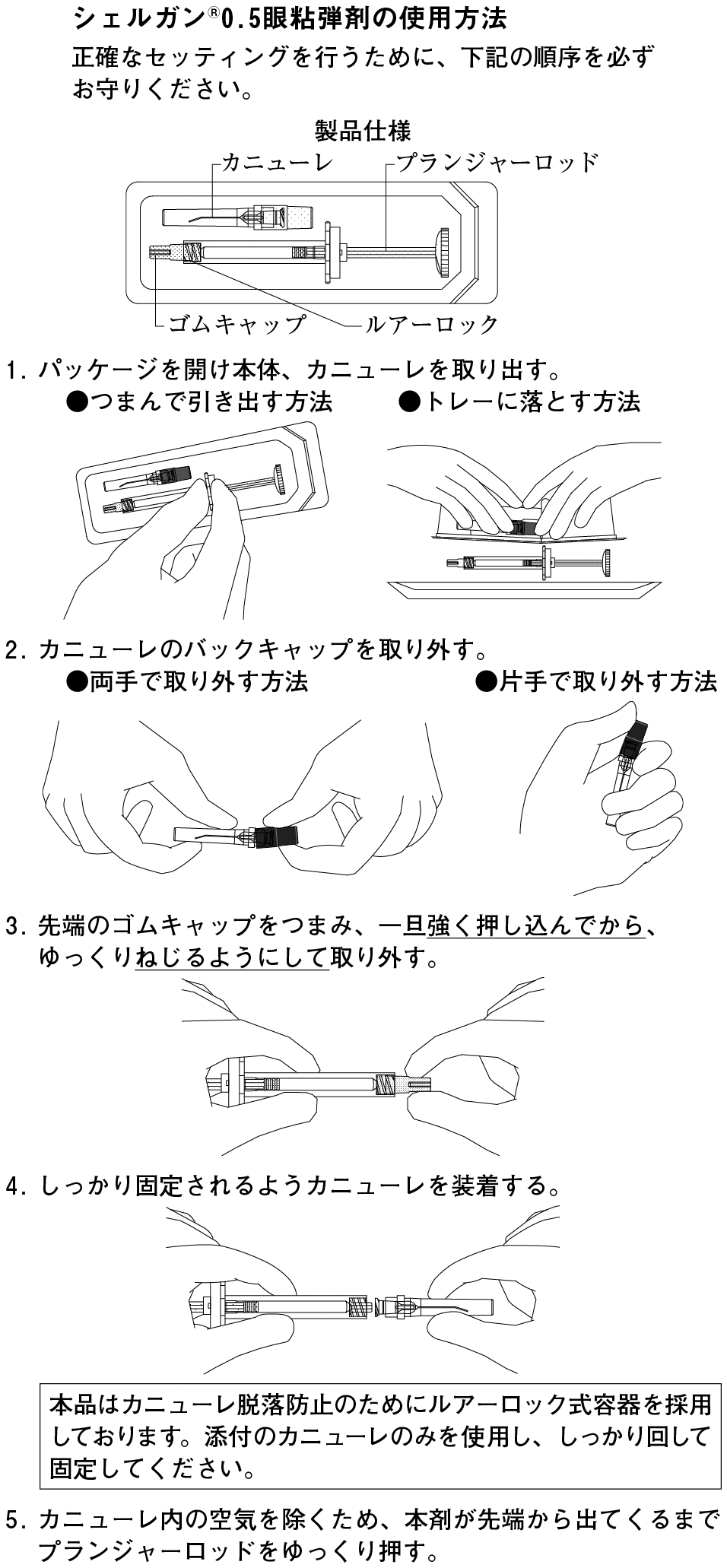
本剤の使用にあたっては、必ず添付のカニューレを使用し、カニューレが完全にシリンジに装着したことを確認してから使用する。装着が完全でないと、使用中にカニューレが外れ重篤な事故が生ずる可能性がある。
注意深く、ゆっくりと注入すること。
過量に注入しないこと。術後の眼圧上昇の原因となる可能性がある。
超音波乳化吸引術を行う前に灌流・吸引を行い、水晶体と本剤との間に灌流液で満たした空間を作ること。空間が不十分なまま超音波乳化吸引を行うとチップの閉塞により、灌流不全となり角膜熱傷を起こすことがある。
特に手術後は、注意深く眼圧を観察すること。もし、眼圧上昇があらわれた場合は適切な処置を行うこと。
手術後、灌流・吸引により本剤を除去すること。ただし、本剤は低凝集性のため、高凝集性の類薬に比べて灌流・吸引に時間を要するので慎重に行うこと。
特定の背景を有する患者に関する注意
合併症・既往歴等のある患者
本剤の成分又は蛋白系薬剤に対し過敏症の既往歴のある患者
治療上やむを得ないと判断される場合を除き、使用は避けること。
小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
その他の副作用
| 0.1~5%未満 | 頻度不明 |
|---|
眼 | 眼圧上昇 | 角膜浮腫、角膜混濁、炎症反応、霧視 |
|---|
適用上の注意
薬剤使用時の注意
本剤の使用にあたっては、気泡の混入を防ぐため使用法に十分留意すること。
術後は本剤を十分に除去すること。
本剤の開封後の使用は1回限りとし、残液は容器とともに廃棄すること。
臨床成績
有効性及び安全性に関する試験
国内第III相試験
超音波乳化吸引法による白内障摘出術及び眼内レンズ挿入術の比較試験214例(精製ヒアルロン酸ナトリウム/コンドロイチン硫酸エステルナトリウム眼粘弾剤群:106例、対照薬(ヒアルロン酸ナトリウム1%製剤)群:108例)において、精製ヒアルロン酸ナトリウム/コンドロイチン硫酸エステルナトリウム眼粘弾剤群では術後12週の角膜内皮細胞減少率は6.5±11.7%(平均値±S.D.)であり、主に手術の容易性と角膜内皮細胞保護効果に基づいて判定された有効率は91.1%(92/101例)であった。有効性と安全性の結果より、有用率は89.1%(90/101例)であった。副作用として、眼圧上昇2.9%(3/104例)が報告された 。
薬効薬理
作用機序
本剤は分散性が高く、超音波乳化吸引術時の灌流・吸引下でも眼内に滞留することで前房空間を保持し、手術時の機械的侵襲や超音波による侵襲から角膜内皮細胞を物理的に保護する。
角膜内皮保護効果
ブタ摘出角膜の内皮に、本剤又はオキシグルタチオン含有眼灌流液(対照群)を100μL滴下し、眼内レンズ素材(ポリメチルメタクリレート)接触後の角膜内皮障害部位面積を指標にした試験により、本剤は統計学的に有意に優れた角膜内皮保護効果を示した (in vitro)。
ウサギ眼球を用いて、本剤又はオキシグルタチオン含有眼灌流液(対照群)で前房水(250μL)を置換後、超音波乳化吸引術後の一定面積当たりの角膜内皮細胞数を指標にした試験により、本剤は統計学的に有意に優れた角膜内皮保護効果を示した (in vivo)。
生物学的同等性試験
本剤と標準製剤の角膜内皮保護効果を生物学的同等性試験にて評価した。ブタ摘出眼球を用いたin vitro試験及びウサギを用いたin vivo試験の結果より、本剤と標準製剤は生物学的に同等の角膜内皮保護効果を示した。
ブタ摘出角膜の内皮に、本剤、標準製剤(ビスコート®0.5眼粘弾剤)又はオキシグルタチオン含有眼灌流液(対照群)を100μL滴下し、眼内レンズ素材(ポリメチルメタクリレート)接触後の角膜内皮障害部位面積を指標に角膜内皮保護効果を評価した(in vitro)。本剤群および標準製剤群の角膜内皮障害部位面積が、対照群と比較して有意水準5%において統計学的に有意に小さく(Satterthwaite t検定、P=0.0004)、かつ両製剤群間の角膜内皮障害部位面積が有意水準15%においても統計学的に有意差を認めなかったことから(t検定、P=0.9248)、本剤群と標準製剤群の生物学的同等性が確認された 。
ウサギ眼球を用いて、本剤、標準製剤(ビスコート®0.5眼粘弾剤)又はオキシグルタチオン含有眼灌流液(対照群)で前房水(250μL)を置換後、超音波乳化吸引術後の一定面積当たりの角膜内皮細胞数を指標に角膜内皮保護効果を評価した(in vivo)。本剤群および標準製剤群の角膜内皮細胞数が、対照群と比較して有意水準5%において統計学的有意に多く((対照群vs標準製剤群;Satterthwaite t検定、P=0.0002)及び(対照群vs本剤群;t検定、P<0.0001))、さらに本剤群と標準製剤群の平均値の差の標準製剤群に対する比率の90%信頼区間を算出したところ、-0.0075(-0.0644~0.0493)であり判定基準(-0.20~0.20)の範囲内であったため、本剤群と標準製剤群の生物学的同等性が確認された 。
有効成分に関する理化学的知見
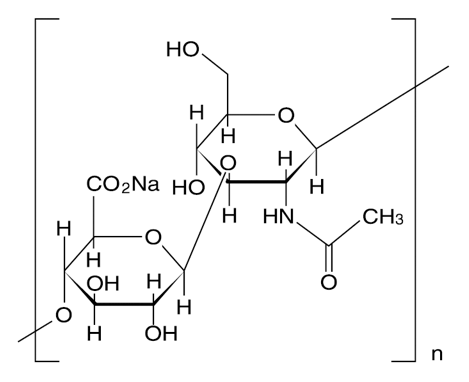
19.1 精製ヒアルロン酸ナトリウム
一般的名称
精製ヒアルロン酸ナトリウム(Purified Sodium Hyaluronate)
分子式
(C14H20NNaO11)n
性状
本品は白色の粉末、粒又は繊維状の塊である。
本品は水にやや溶けにくく、エタノール(99.5)にほとんど溶けない。
本品は吸湿性である。
化学構造式
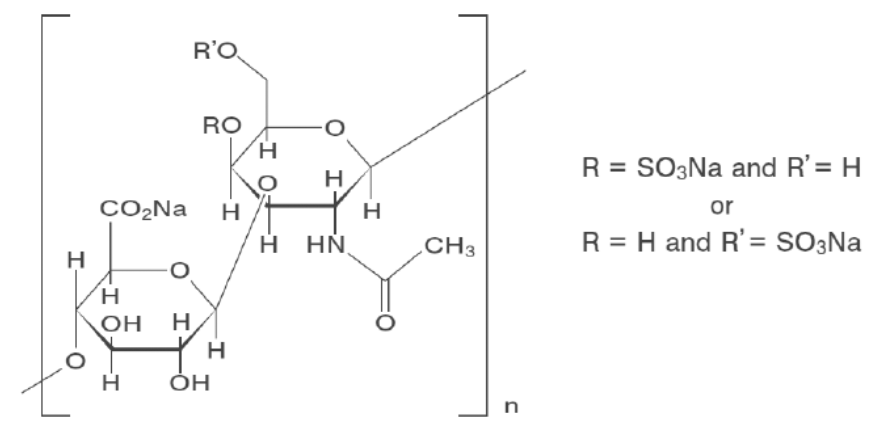
19.2 コンドロイチン硫酸エステルナトリウム
一般的名称
コンドロイチン硫酸エステルナトリウム(Chondroitin Sulfate Sodium)
分子式
(C14H19NNa2O14S)n
性状
本品は白色~微黄褐色の粉末で、においはないか、又はわずかに特異なにおい及び味がある。
本品は水に溶けやすく、エタノール、アセトン又はエーテルにほとんど溶けない。
本品の水溶液(1→100)のpHは5.5~7.5である。
本品は吸湿性である。
化学構造式
取扱い上の注意
ブリスター包装内は滅菌済みのため、使用直前に開封すること。開封後は速やかに使用すること。
ブリスター包装が開封していたり、破損している場合、使用しないこと。
包装
プラスチック製シリンジ入り 0.5mL×1筒
専用ディスポーザブルカニューレ 27G(滅菌済) 1個
主要文献
1
松井瑞夫:日本眼科紀要. 1996; 47(7): 874-891.〔52766〕
2
生化学工業(株)社内資料:生物学的同等性試験〔64948〕
文献請求先及び問い合わせ先
〒530-8552(個別郵便番号) 大阪市北区大深町4-20
製造販売業者等
生化学工業株式会社
東京都千代田区丸の内一丁目6-1