1
田村修 他:Clin. Eval. 1987;15(3):577-599
2
田村修 他:あたらしい眼科. 1988;5(3):453-462
3
北野周作 他:あたらしい眼科. 1987;4(8):1150-1153
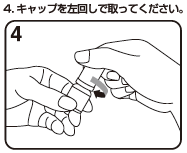
4
大石正夫 他:日眼会誌. 1987;91(1):161-167
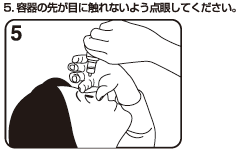
5
石田了三 他:あたらしい眼科. 1993;10(12):2061-2066
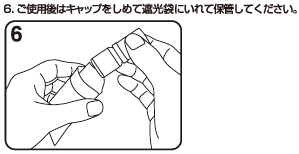
6
平井敬二 他:Chemotherapy. 1990;38(S-2):1-10
7
市川一夫 他:あたらしい眼科. 1988;5(3):431-441
8
調枝寛治 他:あたらしい眼科. 1988;5(3):443-452
9
井上愼三 他:あたらしい眼科. 1988;5(4):593-601
10
中村聡 他:眼科臨床医報. 1987;81(10):2252-2256
11
伊藤明 他:Chemotherapy. 1981;29(S-4):66-82