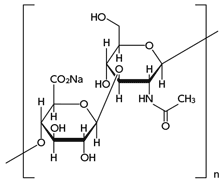
1
第十八改正 日本薬局方解説書 廣川書店 2021;C4223-C4226
2
北野周作 他:日本眼科紀要 1993;44:487-497
3
榛村重人 他:あたらしい眼科 1993;10:611-616
4
糸井素純 他:あたらしい眼科 1993;10:617-626
5
北野周作 他:あたらしい眼科 1993;10:603-610
6
Nakamura, M. et al.:J. Cellular Physiol. 1994;159:415-422
7
Nakamura, M. et al.:Current Eye Res. 1994;13:385-388
8
Nakamura, M. et al.:Cornea. 1993;12:433-436
9
中村雅胤 他:日本眼科紀要 1995;46:1256-1260
10
Nakamura, M. et al.:Current Eye Res. 1992;11:981-986
11
社内資料:生物学的同等性試験(点眼液0.1%、角膜上皮障害モデルに対する効果)
12
社内資料:生物学的同等性試験(点眼液0.3%、角膜上皮障害モデルに対する効果)
13
社内資料:生物学的同等性試験(点眼液0.1%、ドライアイモデルに対する効果)
14
社内資料:生物学的同等性試験(点眼液0.3%、ドライアイモデルに対する効果)