1
血液透析患者における薬物動態の検討(レミッチカプセル:2009年1月21日承認、申請資料概要2.7.6)
2
腹膜透析患者における薬物動態の検討(レミッチカプセル/OD錠/ノピコールカプセル:2017年9月22日承認、審査報告書)
3
代償性肝硬変患者における薬物動態の検討(ノピコールカプセル:2014年12月26日承認、申請資料概要2.7.6.7)
4
Child-Pugh分類グレードBの肝硬変患者における薬物動態の検討(ノピコールカプセル:2014年12月26日承認、申請資料概要2.7.6.8)
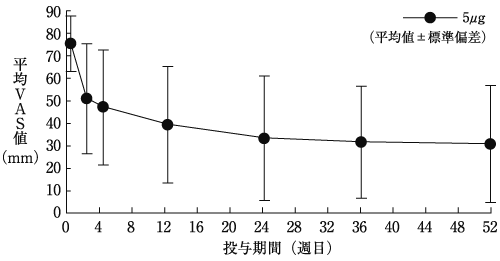
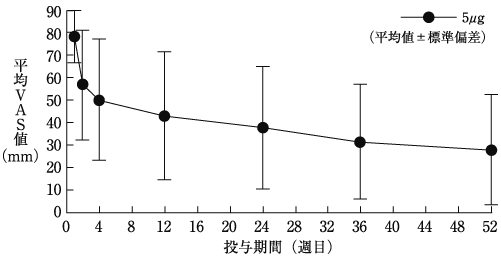
5
竹内譲他:診療と新薬, 2018;55(4):303-314
6
健康成人における食事の影響の検討(レミッチカプセル:2009年1月21日承認、申請資料概要2.7.6)
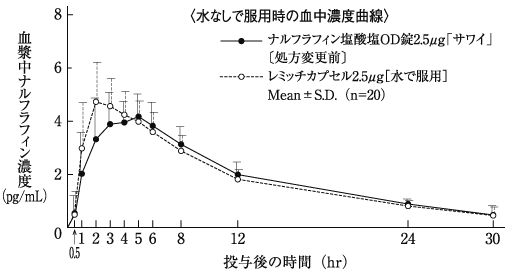
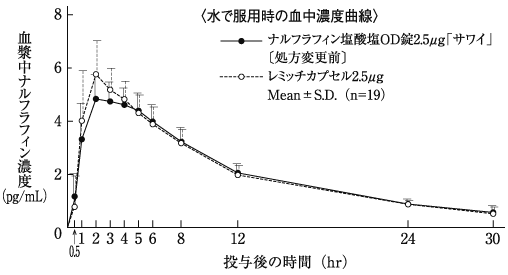
7
中尾薫他:日本薬理学雑誌, 2010;135(5):205-214
8
Ando, A. et al.:Biopharm. Drug Dispos., 2012;33(5):257-264
9
健康成人における吸収、代謝、排泄の検討(レミッチカプセル:2009年1月21日承認、申請資料概要2.7.6)
10
健康成人における薬物相互作用の検討(レミッチカプセル:2009年1月21日承認、申請資料概要2.7.6)
11
薬物相互作用の検討(レミッチカプセル:2009年1月21日承認、申請資料概要2.6.4.7)
12
ヒトP糖タンパク(MDR1)発現LLC-PK1細胞を用いたin vitro試験(ノピコールカプセル:2014年12月26日承認、申請資料概要2.6.4.7)
13
非吸収性薬剤(吸着剤)との薬物相互作用の検討(ノピコールカプセル:2014年12月26日承認、申請資料概要2.6.4.7)
14
非吸収性薬剤(吸着剤)との薬物相互作用の検討(2)(レミッチカプセル/OD錠/ノピコールカプセル:2017年9月22日承認、審査報告書)
15
血液透析の影響(レミッチカプセル:2009年1月21日承認、審査報告書)
16
血液透析患者におけるそう痒症に対する効果の検討(検証的試験)(レミッチカプセル:2009年1月21日承認、申請資料概要2.7.6)
17
血液透析患者におけるそう痒症に対する効果の検討(検証的試験)(レミッチカプセル:2009年1月21日承認、審査報告書)
18
血液透析患者におけるそう痒症に対する効果の検討(長期投与試験)(レミッチカプセル:2009年1月21日承認、申請資料概要2.7.6)
19
腹膜透析患者におけるそう痒症に対する効果の検討(一般臨床試験)(レミッチカプセル/OD錠/ノピコールカプセル:2017年9月22日承認、審査報告書)
20
慢性肝疾患患者におけるそう痒症に対する効果の検討(検証的試験)(ノピコールカプセル:2014年12月26日承認、申請資料概要2.7.6.13)
21
慢性肝疾患患者におけるそう痒症に対する効果の検討(検証的試験)(ノピコールカプセル:2014年12月26日承認、審査報告書)
22
慢性肝疾患患者におけるそう痒症に対する効果の検討(長期投与試験)(ノピコールカプセル:2014年12月26日承認、申請資料概要2.7.6.14)
23
中尾薫他:日本神経精神薬理学雑誌, 2008;28(2):75-83
24
各種受容体、トランスポーターおよびイオンチャネルに対する結合試験(ノピコールカプセル:2014年12月26日承認、申請資料概要2.6.2.2)
25
Umeuchi, H. et al.:Eur. J. Pharmacol., 2003;477(1):29-35
26
Togashi, Y. et al.:Eur. J. Pharmacol., 2002;435(2-3):259-264