1
臨床薬理試験、背景及び概観(ストラテラカプセル:2012年8月24日承認、CTD2.7.2.1)(L20230313)
2
日本人健康成人を対象とした単回投与及び反復投与試験 (ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230314)
3
健康成人と患児の薬物動態の比較(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.3.1.1.3)(L20230315)
4
小児注意欠陥/多動性障害(AD/HD) 患児を対象としたアトモキセチンの安全性及び薬物動態試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230316)
5
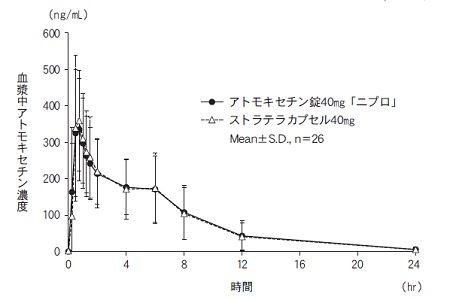
社内資料:生物学的同等性試験(錠40mg)
6
絶対的バイオアベイラビリティ並びにマーロックス®及びオメプラゾール投与時の相対的バイオアベイラビリティについての検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230317)
7
CYP2D6 PM健康成人におけるアトモキセチンのバイオアベイラビリティについてのパイロツト試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230318)
8
バイオアベイラビリティに対する食事の影響 (ストラテラカプセル:2009年4月22日承認、CTD2.7.1.3.3)(L20230319)
9
分布(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.3.1.2)(L20230320)
10
薬物動態(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.3.1)(L20230321)
11
追加の表(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.5.1.3)(L20230322)
12
CYP2D6 分類の変更に伴うLYAN 試験の再解析(ストラテラカプセル:2012年8月24日承認、CTD2.7.2.2.2.1)(L20230323)
13
健康成人における薬物動態(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.3.1.1.1)(L20230324)
14
健康成人における薬物動態及び忍容性試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.2.2)(L20230325)
15
末期腎不全を有する成人にアトモキセチンを単回投与したときの薬物動態の検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230326)
16
薬物動態(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.5.1)(L20230327)
17
肝硬変を有する成人におけるアトモキセチン単回投与後の薬物動態についての検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230328)
18
ヒト生体試料を用いたin vitro 試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.2.2.1)(L20230329)
19
経口メチルフェニデート存在下においてアトモキセチンを反復投与したときの血行力学パラメータに及ぼす影響の検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230330)
20
アトモキセチン併用時におけるサルブタモール吸入投与後の血行力学パラメータの変化についての検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230331)
21
アトモキセチン反復投与時におけるサルブタモール単回静脈内投与後の血行力学パラメータの変化についての検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230332)
22
健康成人を対象としたアトモキセチン及びパロキセチン併用時における安全性及び薬物動態学的相互作用の検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230333)
23
健康成人を対象としたアトモキセチン及びフルオキセチン併用時における安全性及び薬物動態学的相互作用の検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230334)
24
CYP2D6 PM健康成人を対象としたアトモキセチン及びミダゾラム併用時における安全性及び薬物動態学的相互作用の検討(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)(L20230335)
25
CYP2D6 EM 及びPM 健康成人を対象としたアトモキセチン及びエタノール併用時における精神運動作用についての検討(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.2)(L20230336)
26
社内資料:生物学的同等性試験(錠5mg)
27
社内資料:生物学的同等性試験(錠10mg)
28
社内資料:生物学的同等性試験(錠25mg)
29
Takahashi,M.et al.: J.Child Adolesc.Psychopharmacol.2009; 19(4): 341-350(L20201185)
30
アトモキセチン(LY1 39603)の小児における注意欠陥/多動性障害患者に対するプラセボ対照二重盲検比較試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.3)(L20230337)
31
アトモキセチン(LY1 39603)の小児における注意欠陥/多動性障害患者に対する長期継続投与試験中間報告(第2報)(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.3)(L20230338)
32
Michelson,D. et al.: Pediatrics. 2001;108(5,e83):1-9(L20201186)
33
年齢 8~18 歳の小児及び青少年期AD/HD 外来患者を対象として固定用量(mg/kg/日)のアトモキセチンとプラセボの有効性及び安全性を比較する第III相、無作為化、二重盲検、プラセボ対照試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.6.3)(L20230339)
34
用量設定試験:LYAC 試験(ストラテラカプセル:2009年4月22日承認、CTD2.7.4.2.1.1.2.4)(L20230340)
35
成人AD/HD患者に対する第Ⅲ相短期投与プラセボ対照二重盲検比較試験(ストラテラカプセル:2012年8月24日承認、CTD2.5.4.2.3)(L20201187)
36
B4Z-JE-LYEE 試験(ストラテラカプセル:2012年8月24日承認、CTD2.7.6.3.1)(L20230341)
37
成人AD/HD患者に対する第Ⅲ相長期継続投与臨床試験 (ストラテラカプセル:2012年8月24日承認、CTD2.5.4.2.4)(L20210220)
38
B4Z-JE-LYEK 試験(ストラテラカプセル:2012年8月24日承認、CTD2.7.6.4.1)(L20230342)
39
Loghin,C.et al.:Br J Clin Pharmacol. 2013;75(2): 538-549(L20230343)
40
緒言(ストラテラカプセル:2009年4月22日承認、CTD2.6.1)(L20230344)
41
モノアミン取り込み阻害作用(ストラテラカプセル:2009年4月22日承認、CTD2.6.2.2.1.2)(L20230345)
42
受容体結合(ストラテラカプセル:2009年4月22日承認、CTD2.6.2.3.1)(L20230346)
43
Bymaster,FP.et al.: Neuropsychopharmacology. 2002; 27(5): 699-711(L20201188)