1
CYP2D6の遺伝子型の解析(ストラテラカプセル:2012年8月24日承認、申請資料概要2.7.2.1)
2
日本人健康成人を対象とした単回投与及び反復投与試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
3
成人と患児の薬物動態比較(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3)
4
麦谷 歩ほか:診療と新薬.2018;55(9):649-659
5
絶対的バイオアベイラビリティ(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
6
バイオアベイラビリティに対する食事の影響(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.1.3)
7
分布(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3)
8
代謝、薬物相互作用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2、2.7.2.3)
9
外国人 PM 健康成人における薬物動態(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.3、2.7.2.5)
10
日本人健康成人における薬物動態(ストラテラカプセル:2012年8月24日、申請資料概要2.7.2.2)
11
排泄(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.2、2.7.2.3)
12
末期腎不全患者における薬物動態(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2.2、2.7.2.5)
13
肝硬変患者における薬物動態(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
14
薬物相互作用(in vitro)(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.2)
15
経口メチルフェニデート併用における血行力学パラメータに及ぼす影響(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
16
吸入サルブタモール併用における血行力学パラメータの変化(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
17
サルブタモール静脈内投与併用における血行力学パラメータの変化(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
18
パロキセチン併用における安全性及び薬物動態学的相互作用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
19
フルオキセチン併用における安全性及び薬物動態学的相互作用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
20
オメプラゾール及びマグネシウム/アルミニウム水酸化物併用における相対的バイオアベイラビリティ(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
21
ミダゾラム併用における安全性及び薬物動態学的相互作用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
22
エタノール併用における精神運動作用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.2)
23
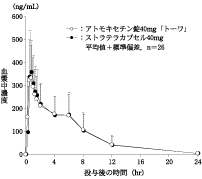
社内資料:生物学的同等性試験(錠5mg)
24
社内資料:生物学的同等性試験(錠10mg)
25
社内資料:生物学的同等性試験(錠25mg)
26
Takahashi M,et al.:J.Child Adolesc.Psychopharmacol.2009;19(4):341-351
27
小児AD/HD患者に対する国内第Ⅱ/Ⅲ相試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.3)
28
小児AD/HD患者に対する第Ⅲ相長期継続投与臨床試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.6.3)
29
Michelson D,et al.:Pediatrics.2001;108(5):e83
30
小児AD/HD患者に対する外国第Ⅲ相試験(ストラテラカプセル:2009年4月22日承認、申請資料概要2.7.4.2、2.7.6.3)
31
成人AD/HD患者に対する第Ⅲ相短期投与プラセボ対照二重盲検比較試験(ストラテラカプセル:2012年8月24日承認、申請資料概要2.5.4.2、2.7.6.3)
32
成人AD/HD患者に対する第Ⅲ相長期継続投与臨床試験(ストラテラカプセル:2012年8月24日承認、申請資料概要2.5.4.2、2.7.6.4)
33
Corina Loghin,et al.:Br J Clin Pharmacol.2013;75(2):538-549
34
作用機序(ストラテラカプセル:2009年4月22日承認、申請資料概要2.6.1)
35
モノアミン取り込み阻害作用(ストラテラカプセル:2009年4月22日承認、申請資料概要2.6.2.2、2.6.2.3)
36
Bymaster FP,et al.:Neuropsychopharmacology.2002;27(5):699-711












 0120-108-932 FAX 06-7177-7379
0120-108-932 FAX 06-7177-7379

