1
健康被験者における薬物動態(空腹時単回投与)(ロナセン錠:2008年1月25日承認、CTD2.7.2.2.2.1)
2
健康被験者における薬物動態(食後単回投与)(ロナセン錠:2008年1月25日承認、CTD2.7.2.2.2.2)
3
単回投与と反復投与後の血漿中濃度の比較(食後反復投与)(ロナセン錠:2008年1月25日承認、CTD2.7.2.3.2)
4
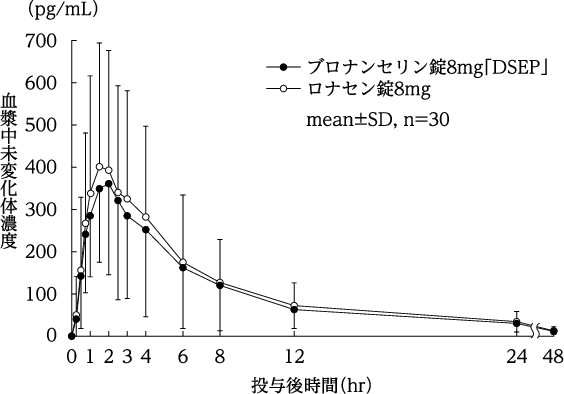
社内資料:生物学的同等性に関する資料
5
ラットの吸収率(ロナセン錠:2008年1月25日承認、CTD2.6.4.3.1.1)
6
ヒト血清蛋白結合(ロナセン錠:2008年1月25日承認、CTD2.7.2.2.1.1)
7
代謝物の薬効関連薬理作用(ロナセン錠:2008年1月25日承認、CTD2.4.2.1.4)
8
代謝経路(ロナセン錠:2008年1月25日承認、CTD2.7.2.2.1.3)
9
代謝物組成(ロナセン錠:2008年1月25日承認、CTD2.4.3.4.2)
10
代謝酵素の同定(ロナセン錠:2008年1月25日承認、CTD2.7.2.2.1.2)
11
14C標識体を用いたマスバランス試験(ロナセン錠:2008年1月25日承認、CTD2.7.2.2.2.1)
12
松本和也ほか:臨床精神薬理 2008;11:891-899
13
薬物動態試験の要約(ロナセン錠:2008年1月25日承認、CTD2.7.2.5)
14
松本和也ほか:臨床精神薬理 2008;11:901-909
15
社内資料:溶出性に関する資料
16
三浦貞則:臨床精神薬理 2008;11:297-314
17
村崎光邦:臨床精神薬理 2007;10:2059-2079
18
ハロペリドールを対照とした第Ⅲ相試験(ロナセン錠:2008年1月25日承認、審査報告書)
19
試験対象集団(ロナセン錠:2008年1月25日承認、CTD2.7.3.3.1)
20
長期投与試験(1)(ロナセン錠:2008年1月25日承認、CTD2.7.6.1.20)
21
村崎光邦:臨床精神薬理 2007;10:2241-2257
22
長期投与試験(2)(ロナセン錠:2008年1月25日承認、CTD2.7.6.1.21)
23
木下利彦:臨床精神薬理 2008;11:135-153
24
長期投与試験(3)(ロナセン錠:2008年1月25日承認、CTD2.7.6.1.22)
25
釆輝昭ほか:臨床精神薬理 2007;10:1263-1272
26
ドパミンD2、D3及びセロトニン5-HT2A受容体に対する作動作用及び拮抗作用(ロナセンテープ:2019年6月18日承認、CTD2.6.2.2.1)
27
代謝物の薬理作用(ロナセン錠:2008年1月25日承認、CTD2.6.2.2.4.1)
28
ムスカリンM3受容体への結合親和性(ロナセンテープ:2019年6月18日承認、CTD2.6.2.2.2)
29
Noda Y, et al.:J Pharmacol Exp Ther. 1993;265:745-751
30
メタンフェタミン誘発運動過多に対する抑制作用(ロナセン錠:2008年1月25日承認、CTD2.6.2.2.1.2)