作成又は改訂年月
**
2017年4月改訂
(第7版,承継に伴う改訂)
*
2011年2月改訂
日本標準商品分類番号
薬効分類名
承認等
販売名
ドロキシドパカプセル100mg「日医工」
販売名コード
承認・許可番号
21800AMZ10301000
Droxidopa
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
気密容器で室温保存
使用期限
外箱等に表示の使用期限内に使用すること
基準名
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
ドロキシドパカプセル100mg「日医工」
1カプセル中ドロキシドパ100mgを含有する。
添加物としてD-マンニトール,トウモロコシデンプン,ステアリン酸マグネシウムを含有する。
また,カプセル本体にゼラチン,酸化チタン,黄色5号,ラウリル硫酸ナトリウムを含有する。
製剤の性状
| だいだい色(キャップ)/白色(ボディ)の硬カプセル剤である。 |
販売名
ドロキシドパカプセル200mg「日医工」
販売名コード
承認・許可番号
21800AMZ10302000
Droxidopa
薬価基準収載年月
販売開始年月
貯法・使用期限等
貯法
気密容器で室温保存
使用期限
外箱等に表示の使用期限内に使用すること
基準名
規制区分
処方箋医薬品
(注意−医師等の処方箋により使用すること)
組成
ドロキシドパカプセル200mg「日医工」
1カプセル中ドロキシドパ200mgを含有する。
添加物としてD-マンニトール,トウモロコシデンプン,ステアリン酸マグネシウムを含有する。
また,カプセル本体にゼラチン,酸化チタン,ラウリル硫酸ナトリウムを含有する。
製剤の性状
禁忌
本剤に対し過敏症の患者
閉塞隅角緑内障の患者[眼圧を上昇させる。]
本剤を投与中の患者には,ハロタン等のハロゲン含有吸入麻酔剤を投与しないこと。(「相互作用」の項参照)
イソプレナリン等のカテコールアミン製剤を投与中の患者(「相互作用」の項参照)
妊婦又は妊娠している可能性のある婦人(「妊婦,産婦,授乳婦等への投与」の項参照)
重篤な末梢血管病変(糖尿病性壊疽等)のある血液透析患者[症状が悪化するおそれがある。]
原則禁忌
コカイン中毒の患者[コカインは神経終末においてカテコールアミンの再取り込みを阻害するため,本剤の作用が増強するおそれがある。]
心室性頻拍のある患者[症状が悪化するおそれがある。]
効能又は効果
効能又は効果に関連する使用上の注意
パーキンソン病への適用にあたっては,次の点に十分留意すること。
Yahr重症度分類でステージIIIと判定された患者であること。
他剤の治療効果が不十分で,すくみ足又はたちくらみが認められる患者にのみ本剤の投与を考慮すること。
血液透析患者への適用にあたっては,次の点に十分留意すること。
透析終了後の起立時に収縮期血圧が15mmHg以上低下する患者であること。なお,本薬の作用機序は不明であり,治療後の血圧低下の減少度は個体内変動を超えるものではない。
○パーキンソン病(Yahr重症度ステージIII)におけるすくみ足,たちくらみの改善
○下記疾患における起立性低血圧,失神,たちくらみの改善
シャイドレーガー症候群,家族性アミロイドポリニューロパチー
○起立性低血圧を伴う血液透析患者における下記症状の改善
めまい・ふらつき・たちくらみ,倦怠感,脱力感
用法及び用量
○パーキンソン病(Yahr重症度ステージIII)におけるすくみ足,たちくらみの改善
通常成人に対し,ドロキシドパとして1日量100mg,1日1回の経口投与より始め,隔日に100mgずつ増量,最適投与量を定め維持量とする(標準維持量は1日600mg,1日3回分割投与)。
なお,年齢,症状により適宜増減するが,1日900mgを超えないこととする。
○下記疾患における起立性低血圧,失神,たちくらみの改善
シャイドレーガー症候群,家族性アミロイドポリニューロパチー
通常成人に対し,ドロキシドパとして1日量200〜300mgを2〜3回に分けて経口投与より始め,数日から1週間毎に1日量100mgずつ増量,最適投与量を定め維持量とする(標準維持量は1日300〜600mg,1日3回分割投与)。
なお,年齢,症状により適宜増減するが,1日900mgを超えないこととする。
○起立性低血圧を伴う血液透析患者における下記症状の改善
めまい・ふらつき・たちくらみ,倦怠感,脱力感
通常成人に対し,ドロキシドパとして1回量200〜400mgを透析開始30分から1時間前に経口投与する。
なお,年齢,症状により適宜減量する。1回量は400mgを超えないこととする。
用法及び用量に関連する使用上の注意
パーキンソン病への適用にあたっては,効果が認められない場合には,漫然と投与しないよう注意すること。
血液透析患者への適用にあたっては,1ヵ月間投与しても効果が認められない場合には,投与を中止すること。
使用上の注意
慎重投与
高血圧の患者[高血圧を悪化させることがある。]
動脈硬化症の患者[過度の昇圧反応が起こるおそれがある。]
甲状腺機能亢進症の患者[頻脈等の症状が悪化するおそれがある。]
重篤な肝又は腎障害のある患者
心疾患のある患者[症状が悪化するおそれがある。]
重篤な肺疾患,気管支喘息又は内分泌系疾患のある患者[これらの症状が悪化するおそれがある。]
慢性開放隅角緑内障の患者[眼圧が上昇するおそれがある。]
重度の糖尿病を合併した血液透析患者[末梢循環障害を生じるおそれがある。]
重要な基本的注意
本剤の投与は,少量から開始し観察を十分に行い慎重に維持量まで増量すること。ただし,その他の抗パーキンソン剤,昇圧剤の投与を中止する必要はない。
過度の昇圧反応を起こすことがあるので,過量投与にならないように注意すること。
血液透析患者への適用にあたっては,次の点に十分留意すること。
用法(透析開始30分から1時間前に経口投与)・用量を遵守し,透析後の追加など過剰投与(過度の昇圧反応が見られることがある)にならないように注意すること。
糖尿病を合併した血液透析患者への適用にあたっては,糖尿病の程度(末梢循環,血圧,血糖管理などの状態や,血管合併症の程度など)に十分留意すること。
相互作用
併用禁忌
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| ハロタン等のハロゲン含有吸入麻酔剤 | 頻脈,心室細動の危険が増大する。 | ハロゲン含有吸入麻酔剤は,心筋のノルアドレナリンに対する感受性を高める。 |
イソプレナリン等のカテコールアミン製剤
イソメニール,
プロタノール等 | 不整脈,場合により心停止を起こすおそれがある。 | 相加的に作用(心臓刺激作用)を増加させる。 |
併用注意
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
| モノアミン酸化酵素阻害剤 | 本剤の作用が増強され,血圧の異常上昇をきたすことがある。 | ノルアドレナリンの代謝が抑制され,ノルアドレナリンの濃度が増加する。 |
三環系抗うつ剤
イミプラミン,
アミトリプチリン等 | 本剤の作用が増強され,血圧の異常上昇をきたすことがある。 | 神経終末でのノルアドレナリンの再吸収が阻害され,ノルアドレナリンの濃度が増加する。 |
分娩促進剤
オキシトシン
エルゴタミン
抗ヒスタミン剤
クロルフェニラミン等 | 本剤の作用が増強され,血圧の異常上昇をきたすことがある。 | 相加的に作用(末梢血管収縮作用)を増強させる。 |
α1-受容体遮断作用のある薬剤
タムスロシン,
ドキサゾシン,
イフェンプロジル等 | 本剤の作用が減弱される可能性がある。 | これらの薬剤はα1受容体遮断作用を有する。 |
| アメジニウム | 本剤の作用が増強され,血圧の異常上昇をきたすことがある。 | 神経終末でのノルアドレナリンの再吸収・代謝が阻害され,ノルアドレナリンの濃度が増加する。 |
レセルピン誘導体
レセルピン等 | 本剤の作用が減弱される可能性がある。 | レセルピンは脳内ノルアドレナリン,ドパミンを減少させる。 |
レボドパ
アマンタジン等 | これらの医薬品の作用を増強することがある。 | 動物実験でレボドパ,アマンタジンの作用を増強することが認められている。 |
フェノチアジン系薬剤
ブチロフェノン系薬剤 | 本剤の作用が減弱することがある。 | これらの薬剤は抗ドパミン作用のほかに末梢のα受容体遮断作用を有する。 |
| *鉄剤 | 本剤の作用が減弱される可能性がある。 | 動物実験でキレートを形成し,本剤の吸収が減少するとの報告がある。 |
副作用
副作用等発現状況の概要
本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
重大な副作用
悪性症候群(Syndrome malin)(頻度不明)
高熱,意識障害,高度の筋硬直,不随意運動,血清CK(CPK)の上昇等があらわれることがあるので,このような場合には,投与開始初期の場合は中止し,また,継続投与中の用量変更・中止時の場合は一旦もとの投与量に戻した後慎重に漸減し,体冷却,水分補給等の適切な処置を行うこと。
白血球減少,無顆粒球症,好中球減少,血小板減少(頻度不明)
観察を十分に行い,異常が認められた場合には,投与を中止し適切な処置を行うこと。
その他の副作用
次のような副作用が認められた場合には,必要に応じ,減量,投与中止等の適切な処置を行うこと。
| | 頻度不明 |
| 精神神経系注1) | 幻覚,妄想,夜間せん妄,神経過敏(いらいら感,焦燥感,興奮等),不随意運動,不安,パーキンソン症状の増悪,抑うつ,知覚異常,精神症状の増悪,悪夢,感情失禁,振戦,固縮,すくみ,言語障害の悪化 |
| 精神神経系 | 頭痛・頭重感,めまい,頭がぼーっとする,眠気,不眠,健忘 |
| 消化器 | 悪心,嘔吐,食欲不振,胃痛(胃部不快感等),口渇,腹痛,消化不良(胸やけ等),便秘,下痢,腹部膨満感,舌のあれ,流涎 |
| 循環器注2) | 血圧上昇,動悸,胸痛(胸部不快感,胸部絞扼感等),不整脈,狭心症,四肢冷感,チアノーゼ |
| 肝臓 | AST(GOT),ALT(GPT),Al-P,LDHの上昇 |
| 過敏症注3) | 発疹,そう痒 |
| 眼 | 羞明 |
| 泌尿器 | 頻尿,尿失禁,尿閉 |
| その他 | 浮腫,倦怠感,ほてり(顔面潮紅等),のぼせ,眼瞼浮腫,脱力感,発汗,発熱,CK(CPK)上昇,両手の痛み,肩こり |
高齢者への投与
一般に高齢者では生理機能が低下しているので過量投与にならないように注意すること。
妊婦,産婦,授乳婦等への投与
妊婦又は妊娠している可能性のある婦人には投与しないこと。[動物実験で胎児の波状肋骨の増加が,また,他剤(dl-ノルアドレナリン)で子宮血管の収縮により胎児が仮死状態となることが報告されている。]
授乳中の婦人には投与を避けることが望ましいが,やむを得ず投与する場合は授乳を避けさせること。[動物実験で乳汁中への移行が,また,母獣への授乳期投与において児の発育抑制が報告されている。]
小児等への投与
低出生体重児,新生児,乳児,幼児又は小児に対する安全性は確立していない。(使用経験が少ない。)
適用上の注意
薬剤交付時
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により,硬い鋭角部が食道粘膜へ刺入し,更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている。)
薬物動態
生物学的同等性試験
ドロキシドパカプセル100mg「日医工」及び標準製剤を,クロスオーバー法によりそれぞれ1カプセル(ドロキシドパとして100mg)健康成人男子に絶食単回経口投与して血漿中未変化体濃度を測定し,得られた薬物動態パラメータ(AUC,Cmax)について90%信頼区間法にて統計解析を行った結果,log(0.8)〜log(1.25)の範囲内であり,両剤の生物学的同等性が確認された。
1)
また,ドロキシドパカプセル200mg「日医工」及び標準製剤をそれぞれ1カプセル(ドロキシドパとして200mg)投与した場合においても,同様に両剤の生物学的同等性が確認された。1)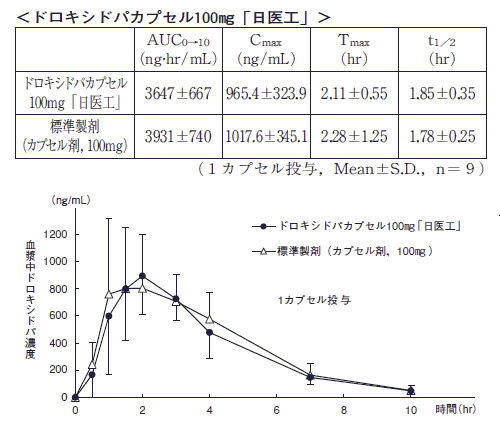
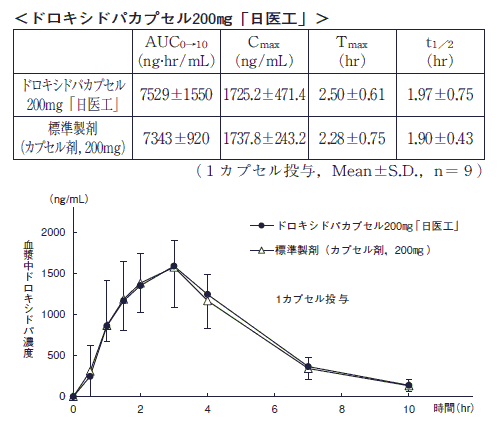
血漿中濃度並びにAUC,Cmax等のパラメータは,被験者の選択,体液の採取回数・時間等の試験条件によって異なる可能性がある。
溶出挙動
ドロキシドパカプセル100mg「日医工」及びドロキシドパカプセル200mg「日医工」は,日本薬局方医薬品各条に定められたドロキシドパカプセルの溶出規格に適合していることが確認されている。2)
薬効薬理
生体内に存在する芳香族L-アミノ酸デカルボキシラーゼにより脱炭酸されてL-ノルアドレナリンとなり,進行したパーキンソン病におけるノルアドレナリン量の減少を補うことにより,パーキンソン病におけるすくみ足や歩行障害に効果を示す。3)
有効成分に関する理化学的知見
一般名
ドロキシドパ(Droxidopa)
化学名
(2
S,3
R)-2-Amino-3-(3,4-dihydroxyphenyl)-3-hydroxypropanoic acid
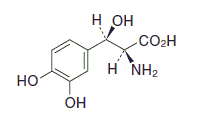
分子式
C9H11NO5
分子量
213.19
性状
白色〜淡褐色の結晶又は結晶性の粉末である。
水に溶けにくく,エタノール(99.5)にほとんど溶けない。
本品は0.1mol/L塩酸試液に溶ける。
取扱い上の注意
安定性試験
本品につき加速試験(40℃,相対湿度75%,6ヵ月)を行った結果,ドロキシドパカプセル100mg「日医工」及びドロキシドパカプセル200mg「日医工」は通常の市場流通下において3年間安定であることが推測された。4)
包装
ドロキシドパカプセル100mg「日医工」
100カプセル(10カプセル×10;PTP)
500カプセル(バラ)
ドロキシドパカプセル200mg「日医工」
100カプセル(10カプセル×10;PTP)
主要文献及び文献請求先
主要文献
1
日医工ファーマ株式会社 社内資料:生物学的同等性試験
2
日医工ファーマ株式会社 社内資料:溶出試験
3
第十六改正日本薬局方解説書 C-3201,廣川書店,東京(2011)
4
日医工ファーマ株式会社 社内資料:安定性試験
文献請求先
主要文献欄に記載の文献・社内資料は下記にご請求下さい。
日医工株式会社 お客様サポートセンター
〒930-8583 富山市総曲輪1丁目6番21
フリーダイアル(0120)517-215
Fax(076)442-8948
製造販売業者等の氏名又は名称及び住所
**販売元
日医工株式会社
富山市総曲輪1丁目6番21
**製造販売元
日医工ファーマ株式会社
富山市総曲輪1丁目6番21
 075
075 075
075
 076
076 076
076

