1
ルネスタ錠:2012年1月18日承認、CTD2.7.6
2
社内資料:エスゾピクロン錠3mg「明治」の生物学的同等性試験に関する資料
3
ルネスタ錠:2012年1月18日承認、CTD2.6.2
4
ルネスタ錠:2012年1月18日承認、CTD2.7.2
5
ルネスタ錠:2012年1月18日承認、審査報告書
6
社内資料:エスゾピクロン錠1mg「明治」の溶出性(生物学的同等性試験)に関する資料
7
社内資料:エスゾピクロン錠2mg「明治」の溶出性(生物学的同等性試験)に関する資料
不眠症治療薬
1錠 18.2円
| 有効成分 | 1錠中エスゾピクロン1mg |
|---|---|
| 添加剤 | 乳糖水和物、結晶セルロース、無水リン酸水素カルシウム、クロスカルメロースナトリウム、ステアリン酸マグネシウム、ヒプロメロース、マクロゴール6000、酸化チタン |
| 有効成分 | 1錠中エスゾピクロン2mg |
|---|---|
| 添加剤 | 乳糖水和物、結晶セルロース、無水リン酸水素カルシウム、クロスカルメロースナトリウム、ステアリン酸マグネシウム、ヒプロメロース、マクロゴール6000、酸化チタン、黄色三二酸化鉄 |
| 有効成分 | 1錠中エスゾピクロン3mg |
|---|---|
| 添加剤 | 乳糖水和物、結晶セルロース、無水リン酸水素カルシウム、クロスカルメロースナトリウム、ステアリン酸マグネシウム、ヒプロメロース、マクロゴール6000、酸化チタン、三二酸化鉄 |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 色調 | 白色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 6.1(mm) 大きさ(厚さ) 2.7(mm) |
| 質量 | 104.5(mg) |
| 剤形 | 割線入りフィルムコーティング錠 |
|---|---|
| 色調 | 淡黄色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 6.1(mm) 大きさ(厚さ) 2.8(mm) |
| 質量 | 104.5(mg) |
| 剤形 | フィルムコーティング錠 |
|---|---|
| 色調 | 淡赤色 |
| 外形 | 表面  裏面  側面  |
| 大きさ | 大きさ(直径) 6.1(mm) 大きさ(厚さ) 2.8(mm) |
| 質量 | 104.5(mg) |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
筋弛緩薬 スキサメトニウム塩化物水和物 ツボクラリン塩化物塩酸塩水和物 パンクロニウム臭化物 中枢神経抑制剤 フェノチアジン誘導体 バルビツール酸誘導体 等 | これらの作用が増強されることがあるので、併用しないことが望ましいが、やむを得ず投与する場合には慎重に投与すること。 | 相加的に抗痙攣作用、中枢神経抑制作用が増強される可能性がある。 |
アルコール(飲酒) | 相互に作用を増強することがある。 | 飲酒により中枢神経抑制作用が増強されることがある。 |
麻酔時 チアミラールナトリウム チオペンタールナトリウム 等 | 呼吸抑制があらわれることがあるので、慎重に投与すること。 | 本剤により呼吸抑制があらわれることがあり、麻酔により相加的に呼吸が抑制される可能性がある。 |
CYP3A4誘導作用を有する薬剤 リファンピシン 等 | 本剤の代謝を促進し、作用を減弱させるおそれがある。 | これらの薬剤の肝代謝酵素誘導作用により、本剤の代謝が促進され、効果の減弱を来すことがある。 |
CYP3A4阻害作用を有する薬剤 イトラコナゾール 等 | 本剤の代謝を阻害し、作用を増強させるおそれがある。 | これらの薬剤の肝代謝酵素阻害作用により、本剤の代謝が阻害され、本剤の血漿中濃度が増加するおそれがある。 |
3%以上 | 1~3%未満 | 1%未満 | 頻度不明 | |
|---|---|---|---|---|
精神神経系 | 傾眠 | 頭痛、浮動性めまい | 不安、注意力障害、異常な夢、うつ病 | 神経過敏、記憶障害、錯感覚、思考異常、感情不安定、錯乱状態 |
過敏症 | 発疹、瘙痒症 | |||
消化器 | 味覚異常 | 口渇 | 口腔内不快感、口内乾燥、下痢、便秘、悪心 | 消化不良、嘔吐 |
肝臓 | AST、ALT、Al-P、γ-GTP、ビリルビンの上昇 | |||
その他 | 倦怠感、湿疹、尿中ブドウ糖陽性、尿中血陽性 | リビドー減退、筋肉痛、片頭痛、背部痛、高血圧、末梢性浮腫 |
投与量 (mg) | 投与 時期 | Cmax (ng/mL) | Tmax (hr) | AUC0-last (ng・hr/mL) | T1/2 (hr) |
1 | 1日目 | 14.52±4.46 | 1.3(0.5-1.5) | 79.60±36.17 | - |
7日目 | 14.71±3.97 | 1.0(0.5-1.5) | 88.71±36.33 | 4.83±0.89 | |
2 | 1日目 | 25.40±7.40 | 1.0(0.5-2.0) | 147.89±57.47 | - |
7日目 | 27.02±5.22 | 1.0(0.5-2.0) | 168.69±67.54 | 5.08±1.62 | |
3 | 1日目 | 37.03±5.70 | 1.5(0.5-2.0) | 222.25±36.95 | - |
7日目 | 37.59±5.54 | 0.8(0.5-2.0) | 252.63±59.17 | 5.16±0.85 |
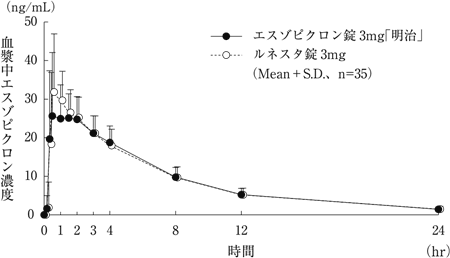
被験 者数 | 判定パラメータ | 参考パラメータ | |||
AUCt (ng・hr/mL) | Cmax (ng/mL) | Tmax (hr) | T1/2 (hr) | ||
エスゾピクロン錠3mg「明治」 | 35 | 213.50±45.85 | 35.54±10.86 | 1.17±1.01 | 5.75±0.67 |
ルネスタ錠3mg | 35 | 216.56±54.81 | 37.07±12.20 | 0.84±0.51 | 5.82±0.75 |
プラセボ | 本剤 | ゾルピデム | ||
2mg | 3mg | |||
評価例数 | 71 | 69 | 68 | 70 |
PSGによる 睡眠潜時 | 22.8 (0.8, 194.5) | 11.3 (0.3, 132.3) p<0.001a) | 10.4 (0.0, 59.3) p<0.001a) | 7.0 (0.0, 146.5) |
主観的 睡眠潜時 | 45.0 (12.5, 210.0) | 25.0 (3.0, 120.0) p<0.001a) | 20.0 (3.0, 142.5) p<0.001a) | 22.5 (0.0, 150.0) |
成人 | 高齢者 | |||
2mg群 | 3mg群 | 1mg群 | 2mg群 | |
ベースライン | 60.0 (15, 240) 84例 | 60.0 (20, 240) 77例 | 60.0 (30, 180) 80例 | 60.0 (15, 240) 83例 |
4週 | 30.0 (0, 180) 81例 | 30.0 (2, 120) 73例 | 30.0 (0, 180) 75例 | 30.0 (2, 90) 79例 |
8週 | 30.0 (5, 90) 79例 | 20.0 (3, 120) 72例 | 22.5 (5, 150) 72例 | 30.0 (3, 90) 75例 |
12週 | 30.0 (0, 120) 75例 | 20.0 (5, 150) 69例 | 20.0 (5, 90) 70例 | 20.0 (5, 90) 74例 |
16週 | 20.0 (0, 120) 72例 | 20.0 (5, 120) 67例 | 20.0 (5, 90) 67例 | 25.0 (5, 120) 73例 |
20週 | 25.0 (1, 120) 70例 | 20.0 (0, 300) 66例 | 20.0 (5, 120) 69例 | 20.0 (5, 90) 74例 |
24週 | 20.0 (0, 120) 70例 | 20.0 (5, 240) 65例 | 20.0 (5, 180) 68例 | 20.0 (5, 90) 72例 |
最終評価時 | 27.5 (0, 240) 84例 | 20.0 (3, 240) 75例 | 20.0 (5, 180) 79例 | 20.0 (5, 120) 83例 |
プラセボ | 本剤 | ゾルピデム | ||
2mg | 3mg | |||
評価例数 | 63 | 63 | 64 | 64 |
PSGによる 睡眠潜時 | 29.0 (1.5, 143.5) | 15.5 (1.8, 99.5) P≦0.0001a) | 13.1 (0.5, 91.3) P≦0.0001a) | 13.1 (1.0, 81.0) |
成人 | ||||
プラセボ | 2mg | 3mg | ||
試験1 (44日間、1、15及び29日目の平均値) | 評価例数 | 99 | 104 | 105 |
PSGによる 睡眠潜時 (分) | 29.0 (1.0, 131.9) | 15.0 (0.8, 164.0) p<0.0001a) | 13.1 (0.8, 85.3) p<0.0001a) | |
試験2 (6ヵ月間、4~6ヵ月の平均値) | 評価例数 | 172 | 543 | |
主観的 睡眠潜時 (分) | 44.8 (4.1, 330.0) | 31.7 (2.1, 565.0) p<0.0001a) | ||
試験3 (6ヵ月間、4~6ヵ月の平均値) | 評価例数 | 226 | 504 | |
主観的 睡眠潜時 (分) | 45.0 (4.0, 315.0) | 27.3 (3.4, 196.7) p<0.0001a) | ||
高齢者 | ||||
プラセボ | 1mg | 2mg | ||
試験4 (14日間、1、2、13、14日目の平均値) | 評価例数 | 128 | 136 | |
PSGによる 睡眠潜時 (分) | 30.4 (4.1, 173.1) | 14.8 (2.0, 102.1) p<0.0001a) | ||
睡眠効率 (%) | 74.6 (24.7, 91.6) | 80.4 (59.3, 92.3) p<0.0001a) | ||
試験5 (14日間の平均値) | 評価例数 | 79 | 70 | 79 |
主観的 睡眠潜時 (分) | 52.0 (4.7, 540.0) | 35.9 (0.0, 348.0) p=0.0120a) | 36.2 (5.4, 410.0) p=0.0034a) | |